微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组物质之间的反应,调节反应物用量,离子方程式不变的是 ( )
A.稀硝酸和Fe
B.NaAlO2溶液和盐酸
C.AlCl3溶液和氨水
D.CO2通入NaOH溶液
参考答案:C
本题解析:略
本题难度:一般
2、选择题 下列离子方程式中正确的是
A.稀硫酸与氢氧化钡溶液反应 Ba2++SO42-=BaSO4↓
B.铝与氢氧溶液化钠反应 Al+2OH-=AlO2-+H2↑
C.向Na2CO3浓溶液中缓慢滴加几滴稀盐酸 CO32-+H+=HCO3-
D.锌粒与稀醋酸反应 Zn+2H+= Zn2++H2↑
参考答案:C
本题解析:
试题分析:A项应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,错误;B项应为2H2O+2Al+2OH-=2AlO2-+3H2↑,错误;D项醋酸为弱酸所以不能用H+表示,错误。
考点:离子方程式的书写。
本题难度:一般
3、选择题 下列离子方程式正确的是
A.1mol Cl2通入含有2mol FeI2的溶液中:2Fe2++2I
参考答案:
本题解析:
本题难度:一般
4、填空题 (22分)现有下列九种物质:
①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:
分类标准
| 能导电
| 非电解质
| 电解质
|
属于该类的物质
|
|
|
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-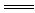 H2O,该离子反应对应的化学方程式为 。 H2O,该离子反应对应的化学方程式为 。
(3)⑨在水中的电离方程式为 ,
34.2g⑨溶于水配成250mL溶液, SO42-的物质的量浓度为 。
(4)少量的④通入⑥的溶液中反应的离子方程式为: 。
(5)将②加入NaOH的溶液中反应的离子方程式
(6)②与⑧发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是
(填化学式),还原剂与氧化剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。
参考答案:19.(1) ②⑦⑧⑨ ④ ③⑤⑥⑨
本题解析:
本题难度:一般
5、推断题 (13分)某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
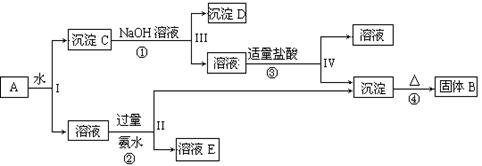
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出下列B、D所含物质的化学式
固体B ;沉淀D 。
(3)写出①、②反应的离子方程式:
① ;② ;
(4)以Fe2O3为原料,可制备FeCl2溶液,请写出有关的化学反应方程式,试剂任选。
参考答案:(1)过滤 (1分)
(2)Al2O3;(2分) Fe
本题解析:
试题分析:由流程可知,Al2O3和Fe2O3不溶于水,则沉淀C为Al2O3和Fe2O3,氧化铁与碱不反应,则沉淀D为Fe2O3,反应②③中生成的沉淀为Al(OH) 3,受热分解生成B为Al2O3,反应②为KAl(SO4)2与氨水的反应,则溶液E为K2SO4、(NH4)2SO4、NH3・H2O,(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离方法为过滤;(2)由上述分析可知,B为Al2O3,D为Fe2O3;(3)反应①为Al2O3+2OH-=2AlO2-+H2O,反应②为Al3++3NH3・H2O=Al(OH) 3↓+3NH4+;(4)以Fe2O3为原料,可制备FeCl2溶液,可以由Fe2O3与盐酸反应产生FeCl3,再加入铁粉使FeCl3转化为FeCl2,则相关反应方程式为:Fe2O3 + 6HCl =" 2" FeCl3 + 3 H2O;2FeCl3 + Fe = 3FeCl2 。
考点:考查无机物的推断。
本题难度:困难
|