微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8 分)写出下列各离子反应方程式
(1)铝和氢氧化钠的反应
(2)氢氧化铝和盐酸的反应
(3)钠和盐酸的反应
(4)钠和硫酸铜的反应
参考答案:(每空2分)(1)2Al+2OH-+2H2O=2![]()
本题解析:
试题分析:铝能和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式是2Al+2OH-+2H2O=2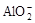 +3H2;氢氧化铝是两性氢氧化物,和盐酸反应的离子方程式是Al(OH)3+3H+=A13++3H2O;钠和盐酸反应生成氢气,反应的离子方程式是2Na+2H+=2 Na++H2;由于钠和水反应生成氢气和氢氧化钠,然后生成的氢氧化钠再和硫酸铜反应生成氢氧化铜,反应的离子方程式是2Na+2H2O=2Na++2OH-+H2、Cu2+ + 2OH― = Cu(OH)2↓。
+3H2;氢氧化铝是两性氢氧化物,和盐酸反应的离子方程式是Al(OH)3+3H+=A13++3H2O;钠和盐酸反应生成氢气,反应的离子方程式是2Na+2H+=2 Na++H2;由于钠和水反应生成氢气和氢氧化钠,然后生成的氢氧化钠再和硫酸铜反应生成氢氧化铜,反应的离子方程式是2Na+2H2O=2Na++2OH-+H2、Cu2+ + 2OH― = Cu(OH)2↓。
考点:考查离子方程式的书写
点评:用实际参加反应的离子表示的方程式是离子方程式。书写离子方程式的关键是准确判断出哪些物质用化学式表示,哪些物质用离子符号表示。只有同时满足易溶、易电离的物质才能用离子表示,其余全部是用化学式表示,据此可以进行有关的书写和判断。
本题难度:一般
2、选择题 下列离子方程式或化学方程式与所述事实相符且正确的是
A.硫酸与氢氧化钡反应的中和热化学反应方程式为: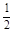 H2SO4(aq)+
H2SO4(aq)+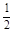 Ba(OH)2(aq)=
Ba(OH)2(aq)=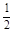 BaSO4(s)+H2O(l) ΔH=-57.3 kJ/mol
BaSO4(s)+H2O(l) ΔH=-57.3 kJ/mol
B.向0.1 mol・L-1、pH=1的NaHA溶液中加入NaOH溶液:H++OH-=H2O
C.以金属银为阳极电解饱和硫酸铜溶液:2Cu2++2H2O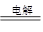 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
参考答案:B
本题解析:
试题分析:A、由于反应中生成的硫酸钡存在溶解平衡,溶解是吸热的,则反应热不可能是-57.3 kJ/mol,A错误;B、0.1 mol・L-1、pH=1的NaHA溶液,这说明NaHA完全电离,属于强电解质,则与NaOH溶液反应的离子方程式可表示为H++OH- =H2O,B正确;C、金属银作阳极,则银失去电子转化为银离子,方程式错误,C不正确;D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀时恰好生成氢氧化铝和一水合氨,离子方程式不正确,D错误,答案选B。
考点:考查方程式的正误判断
本题难度:困难
3、填空题 (12分)卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性质,查阅资料并进行实验。
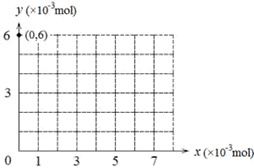
查阅资料如下:
①BrO3-+ 6I-+ 6H+ = 3I2 + Br-+ 3H2O ② 2BrO3-+ I2 = 2IO3-+ Br2
③ IO3-+ 5I-+ 6H+ = 3I2 + 3H2O ④ 2IO3-+ 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
步 骤
| 现 象
|
参考答案:
本题解析:
本题难度:困难
4、选择题 下列离子方程式书写正确的是
A.向氯化铁溶液中加入铁:Fe3+ + Fe = 2Fe2+
B.向AlCl3溶液中加入足量的氨水:Al3++ 4OH-= AlO2- + 2H2O
C.铜与稀硝酸的反应:3Cu + 8H++ 2NO3- =3Cu2+ + 2NO↑+ 4H2O
D.氯气和水的反应:Cl2 + H2O = 2H+ + Cl- + ClO-
参考答案:C
本题解析:
试题分析:A、电荷不守恒,错误;B、氢氧化铝不溶于氨水,发生的反应:Al3++3NH3・H2O=Al(OH)3↓+3NH4+,错误;C、铜与稀硝酸反应:3Cu+8HNO3=2Cu(NO3)2+2NO↑+4H2O,离子反应方程式:3Cu + 8H++ 2NO3- = 3Cu2+ + 2NO↑+ 4H2O,正确;D、HClO是弱酸,不能拆写,错误;
考点:考查离子反应方程式的判断。
本题难度:一般
5、选择题 在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是
A.在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32-
B.含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D.在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+
参考答案:A
本题解析:
试题分析:A、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液,硫酸氢钠电离产生的氢离子先与氢氧根离子反应,若再与亚硫酸根离子先反应生成的二氧化硫溶于水使溶液显酸性,又与偏铝酸根离子反应生成氢氧化铝沉淀和亚硫酸根离子,实际相当于先与偏铝酸根离子反应,最后与亚硫酸根离子反应,正确;B、根据离子的还原性的强弱,判断氯气先与碘离子反应,再与亚铁离子反应,最后与溴离子反应,错误;C、二氧化碳通入混合液中,先与氢氧根离子反应生成碳酸根离子,由于溶液中存在钡离子,所以生成碳酸钡沉淀,实质相当于先与氢氧化钡反应,再与氢氧化钾反应,再与碳酸钾、碳酸钡反应,错误;D、氢氧根离子先与氢离子反应,因为铵根离子与强碱溶液反应。而此时溶液呈弱酸性,所以氢氧根离子再与铁离子反应,最后与铵根离子反应,错误,答案选A。
考点:考查离子反应的顺序的判断
本题难度:一般
|