微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某化学反应反应物的总能量大于生成物的总能量,则该反应
A.是吸热反应
B.是放热反应
C.不一定遵循质量守恒定律
D.不需要加热就一定能发生
参考答案:B
本题解析:
试题分析:反应是放热反应还是吸热反应,与反应条件无关系,只与反应物总能量和生成物总能量的相对大小有关系。如果反应物的总能量高于生成物的总能量,反应就是放热反应,反之是吸热反应。某化学反应反应物的总能量大于生成物的总能量,则该反应是放热反应,选项B正确,AD不正确。化学反应一定遵循质量守恒定律和能量守恒定律,C不正确,答案选B。
点评:该题是基础性试题的考查,侧重对学生教材基础知识的检验,旨在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确放热反应和吸热反应的含义以及判断依据,并能
本题难度:一般
2、选择题 参照反应Br+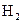 ?
? HBr+H的能量对反应历程的示意图,下列叙述中正确的是
HBr+H的能量对反应历程的示意图,下列叙述中正确的是
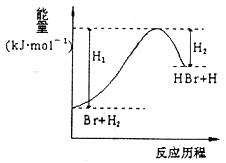
A.正反应为放热反应
B.HBr能量一定高于H2的能量
C.增大反应容器的压强对反应速率没有影响
D.该反应正反应为储能过程
参考答案:D
本题解析:略
本题难度:简单
3、选择题 中和热测定实验中,下列操作一定会降低实验准确性的是
A?用滴定管(精量仪器,读数保留到0.01)取所用酸碱溶液的体积
B? NaOH溶液在倒入小烧杯时,有少量溅出
C、大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多
D、测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度
参考答案:B
本题解析:A正确,滴定管的精确高,可准确量取溶液的体积;B错,NaOH溶液在倒入小烧杯时,有少量溅出导致碱的量不足,反应测定出溶液温度变化量减少,即所测中和热的数值将减小;C正确,保温效果越好,实验的准备性越高;D正确,若不洗将,将会损失酸与碱的量,导致所测中和热的值减小,所以,必须洗净后再来测NaOH溶液的温度。
本题难度:一般
4、选择题 一种化学冰袋含有Na2SO4?10H2O和NH4NO3,用时将它们混合并用手搓揉就可制冷,且制冷效果能维持一段时间.以下关于其制冷原因的推测中肯定错误的是( )
A.Na2SO4?10H2O脱水是吸热过程
B.较长时间制冷是由于Na2SO4?10H2O脱水过程较慢
C.Na2SO4?10H2O在该条件下发生的复分解反应是吸热反应
D.NH4NO3溶于水会吸收热量
参考答案:A、Na2SO4?10H2O脱水是吸热过程,故A正确;
本题解析:
本题难度:简单
5、选择题 下列与化学反应能量变化相关的叙述正确的是[???? ]
A.生成物能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.根据盖斯定律,可计算某些难以直接测定的反应焓变
D.同温同压下,H2(g) + Cl2(g)=2HCl(g)在光照和点燃条件的△H不同
参考答案:C
本题解析:
本题难度:一般