微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 为探究Fe3+和Cu2+对H2O2分解反应的催化效果,某同学分别设计了图1、图2所示的实验。下列叙述中不正确的是
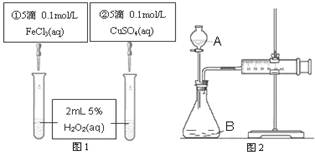
A.图2中的A为分液漏斗
B.图2实验可通过测定相同状况下产生的气体体积与反应时间来比较反应速率
C.若图1实验中反应速率为①>②,则Fe3+对H2O2分解的催化效果一定比Cu2+好
D.图1实验可通过观察产生气泡的快慢来比较反应速率
参考答案:C
本题解析:A.图2中的A为分液漏斗,正确;B.反应速率可用单位时间内产生的气体体积表示,该装置可通过注射器活塞的位置变化看生成气体的体积,所以正确.C.催化剂能改变化学反应的速率,这里是加快速率,若图1所示实验中反应速率为①>②,则一定说明氯化铁比硫酸铜催化效果好,因二者所含的阴离子不同,要证明Fe3+比Cu2+对H2O2分解催化效果好,还要使选择的试剂中阴离子种类相同,所以错误.D.图1实验可通过观察产生气泡的快慢来比较反应速率,正确。
本题难度:一般
2、选择题 下列事实不能用勒夏特列原理来解释的是
A.加压有利于SO2与O2反应生成SO3
B.温度过高对合成氨反应不利
C.高温及加入催化剂都能使合成氨的反应速率加快
D.用过量空气煅烧硫铁矿可以提高原料的利用率
参考答案:C
本题解析:
试题分析:SO2与O2反应生成SO3是一个气体系数减小的反应,加压平衡正向移动可以生成更多的SO3,所以A正确;合成氨的反应是放热反应,所以温度过高平衡逆反应方向移动,不利于氨气合成,B正确;温度、催化剂都能使反应速率加快,但不是勒夏特列原理,C错误;用过量的氧气,相当于增大反应物氧气的浓度,平衡正向移动,硫铁矿的转化率增大,所以D正确。选C。
本题难度:一般
3、选择题 本题列举的四个选项是4位同学在学习“化学反应的速率和化学平衡“一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
A.化学反应速率理论是研究怎样在一定时间内快出产品
B.化学平衡理论是研究怎样使用有限原料多出产品
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使原料尽可能多地转化为产品
参考答案:从工业生产的实际出发,外界条件只影响化学反应速率的大小,不影
本题解析:
本题难度:一般
4、选择题 燃烧硫铁矿产生SO2 ,为了提高生成SO2的速率,下列措施可行的是(???)
A.把块状矿石碾成粉末
B.降低O2的浓度
C.使用负催化剂
D.降低温度
参考答案:A
本题解析:为了提高生成SO2的速率,把块状矿石碾成粉末增大其接触面积,.降低O2的浓度
、使用负催化剂、降低温度都是减小速率。
本题难度:简单
5、选择题 用铁片与稀硫酸制取氢气时,下列措施能使氢气生成速率减缓的是( )
A.使用更稀的硫酸溶液
B.加热
C.滴加少量CuSO4溶液
D.不用铁片,改用铁粉
参考答案:A.使用更稀的硫酸溶液,反应物浓度减小,反应速率降低,故A选
本题解析:
本题难度:简单