��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� 373Kʱ��ij 1L�ܱ������м���1molPCl5�������¿��淴Ӧ�� ��������PCl3�����ʵ����仯����ͼ��ʾ��
��������PCl3�����ʵ����仯����ͼ��ʾ��
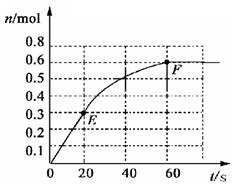
��1 ��ǰ 20
��ǰ 20 s�� PCl5��g����ƽ����Ӧ����Ϊ??????
s�� PCl5��g����ƽ����Ӧ����Ϊ??????
��2��373Kʱ�÷�Ӧ��ƽ�ⳣ����ֵΪ???????
��3�����ڴ�ƽ����ϵ���ټ��� 1mol�� PCl5����ԭƽ��Ƚϣ���ƽ��ʱ PCl5��ת����???�������С������ͬ����PCl5��ƽ��Ũ��???????????????????��
��4����ԭƽ�������� 473K�����´�ƽ��ʱ�������������䣩��PCl3��ƽ��Ũ��Ϊ PCl5��3�����÷�Ӧ������ӦΪ������ȷ�Ӧ���� �����ȷ�Ӧ����????????��Ϊ����ƽ����ϵ�� Cl2�����ʵ��������д�ʩ��ȷ���ǣ�����������ͬ��?????
a.�����¶�???????????????????????????? b.�������������
c.������ʵĴ���???????????????????? d.�ٳ��� PCl3
�ο��𰸣���1�� 0 �����������
�����������
�����Ѷȣ���
2������� ���ǵ�ѭ���е���Ҫ���ʣ����ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵�������
(1)��֪��H��H����Ϊ436 kJ��mol��1��N��N����Ϊ946 kJ��mol��1��N��H����Ϊ391 kJ��mol��1��д���ϳɰ���Ӧ���Ȼ�ѧ����ʽ��????????????????????????????????????????????????????????????
(2)�����£���һ��4L���ܱ������г���5.2molH2��2molN2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±���ʾ��
ʱ��/min
| 5
| 10
| 15
| 20
| 25
| 30
|
c(NH3)/mol��L��1
| 0.08
| 0.14
| 0.18
| 0.20
| 0.20
| 0.20
��5min�ڣ�����H2��ƽ����Ӧ����Ϊ___________________________________?????
��N2��ƽ��ת����???????????????????????????????????????????????????
�۴������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K=__________________________����Ӧ�ﵽƽ�����ά������������䣬�¶Ȳ��䣬��ƽ����ϵ�м���H2��N2��NH3��8mol����ѧƽ�⽫��_______�����ƶ�(�����Ӧ�����淴Ӧ��)��
����ά������������䣬ֻ�����¶Ȼ�ѧƽ�ⳣ��ֵ?????������С�����䣩������Ӧ����?????������С�����䣩��
�����¶�ά�ֲ��䣬ֻ�����������4L��Ϊ2L������ƽ��ʱN2��ƽ��Ũ��????0.4 mol��L��1������ڡ�С�롢���ڣ�
�ο��𰸣�(1)N2(g)? +? 3H2(g)  ����������� �����������
�����Ѷȣ�һ��
3��ѡ���� ��Ӧ4NH3+5O2?4NO+6H2O��5L���ܱ������н���30s��NO�����ʵ���������0.3mol����˷�Ӧ��ƽ������Ϊ��������
A��v��O2��=0.01?mol?L-1?s-1
B��v��NO��=0.008?mol?L-1?s-1
C��v��H2O��=0.003?mol?L-1?s-1
D��v��NH3��=0.002?mol?L-1?s-1
�ο��𰸣���5L���ܱ������н���30s��NO�����ʵ���������0.3m
���������
�����Ѷȣ���
4��ѡ���� ��֪H2��g����I2��g�� 2HI��g������H��0������ͬ�ݻ����ܷ��������ң����м���H2��I2��0��1mol�����м���0��1mol H2��0��2molI2����ͬ�¶��·ֱ�ﵽƽ�⡣����˵������ȷ���� 2HI��g������H��0������ͬ�ݻ����ܷ��������ң����м���H2��I2��0��1mol�����м���0��1mol H2��0��2molI2����ͬ�¶��·ֱ�ﵽƽ�⡣����˵������ȷ����
A�����з�Ӧ���ʱȼ��з�Ӧ���ʿ�
B��ƽ��ʱ�ס����������л����������ʵ���֮��Ϊ2�U3
C����ƽ��ʱ����H2��ת����Ϊ40����������H2��ת���ʴ���40��
D��ƽ����������ټ���0��1mol H2�������µ�ƽ��ʱ��������H2�İٷֺ�������ͬ
�ο��𰸣�D
������������⿼�黯ѧƽ���Ӱ�����ؼ��йؼ��㡣����I2Ũ�ȱȼ��д�Ӧ���죬A��ȷ��H2��g����I2��g�� 2HI��g���ǵ������Ӧ��ƽ��ǰ������ʵ������䣬��ƽ��ʱ�ס����������л����������ʵ���֮��Ϊ2�U3��B��ȷ������I2Ũ�ȱȼ��д�����H2��ת���ʴ���40����C��ȷ��ƽ����������ټ���0��1mol H2�������µ�ƽ�������ƽ��Ϊ��Чƽ�⣬������H2�İٷֺ�����ͬ��D����ȷ�� 2HI��g���ǵ������Ӧ��ƽ��ǰ������ʵ������䣬��ƽ��ʱ�ס����������л����������ʵ���֮��Ϊ2�U3��B��ȷ������I2Ũ�ȱȼ��д�����H2��ת���ʴ���40����C��ȷ��ƽ����������ټ���0��1mol H2�������µ�ƽ�������ƽ��Ϊ��Чƽ�⣬������H2�İٷֺ�����ͬ��D����ȷ��
�����Ѷȣ�һ��
5��ѡ���� һ���¶������£��ڹ̶�������ܱ������з�����ӦA��s��+ 2B��g�� C��g��+ D��g������˵���÷�Ӧ�ﵽƽ��״̬�ı�־�� C��g��+ D��g������˵���÷�Ӧ�ﵽƽ��״̬�ı�־��
A��ƽ����ϵ����ѹ����
B��ƽ���������ƽ����Է�����������
C��C ��D�����ʵ������
D��ƽ��������������ʵ�������
�ο��𰸣�B
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬����Ӧǰ������Dz���ģ����ѹǿ�������ܵ���֪��ʼ���Dz���ģ�AD����ȷ���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ�����ʵ������䣬�������DZ仯�ģ�����B����˵����ƽ��ʱŨ�Ȳ��ٷ����仯��������֮���Ũ�Ȳ�һ����Ȼ�����ij�ֹ�ϵ��C����ȷ����ѡB��
�����Ѷȣ�һ��
|