微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 现有1 L?0.5mol/L的硫酸钠溶液,有关溶液的叙述正确的是( ????)。
A.取0.5 L溶液,Na+的浓度是0.5 mol/L
B.取0.1 L溶液稀释至l L,SO42-离子浓度是0.05 mol/L
C.溶质的离子总数是6.02 x 1023个
D.该溶液是把0.5 mol Na2SO4溶于1 L水中配制而成的
参考答案:B
本题解析:
试题分析:0.5mol/L的硫酸钠溶液中钠离子的浓度是0.5mol/L×2=1mol/L。又因为溶液是均一稳定的,所以A中钠离子的浓度仍然是1mol/L,A错误;0.1 L溶液稀释至l L,SO42-离子浓度变为0.5mol/L÷10=0.05mol/L,所以选项B正确;硫酸钠的物质的量是0.5mol,离子的总物质的量是1.5mol,C不正确;D不正确,因为溶液的体积不是1L,答案选B。
点评:该题是中等难度的试题,试题基础性强,侧重能力的考查和解题方法的指导。有助于培养吸收的逻辑思维能力和
本题难度:简单
2、选择题 常温下,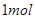 纯水中所含氢离子的物质的量为
纯水中所含氢离子的物质的量为
A.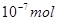
B.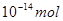
C.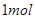
D.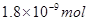
参考答案:D
本题解析:Kw=c(H+)c(OH-),又因水电离的c(H+)=c(OH-),故c(H+)=10-7mol/L,1mol水,18g,18ml,n(H+)=0.018L×10-7mol/L=1.8×10-9mol。
本题难度:一般
3、填空题 (12分)(1)氢能源是21世纪极具有发展前景的新能源之一,它既是绿色能源,又可循环使用。请在下图的每个空格中填上循环过程中反应物和生成物的分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在):
①_____,②_____。从能量转换的角度看,过程Ⅱ应是____能转化为_____能。
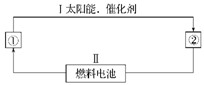
(2)图中的燃料电池也可以用A和氧气为原料。已知A分子是由碳和氢两元素的原子构成,并且8.00 g A中含有3.01×1023个分子。实验测得在298 K时,1 mol该气体完全燃烧生成液态水和二氧化碳,放出890 kJ的热量。
①写出该气体的化学式:______。
②写出1 mol该气体燃烧时的热化学反应方程式:_____________。
③已知1 mol液态的水变成气态水时需要吸收44 kJ的热量,则1 mol该气体完全燃烧生成气态水和二氧化碳时放出的热量为________kJ。
④若该燃料电池中的电解质溶液为氢氧化钾溶液,则:电池正极反应为______________。
参考答案:(12分)
(1)①H2O? ②H2和O2 ??化学?
本题解析:(1)水在太阳能作用下分解为氢气和氧气,而氢气和氧气通过发生原电池反应产生电能,同时生成水。
(2)①由题意很容易可知A的式量为16,属于烃,也只能为甲烷;
②CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ/mol
③H2O(l)= H2O(g)?ΔH=+44 kJ/mol,将③+2×②,可得:
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-802 kJ/mol
④氧气得电子
本题难度:一般
4、选择题 反应A2+B2 2AB在不同温度和压强改变条件下,产物AB的生成情况,如图所示:a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是(???)
2AB在不同温度和压强改变条件下,产物AB的生成情况,如图所示:a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是(???)

A.A2、B2、AB均为气体,正反应放热
B.AB为气体,A2、B2中最少有一种为非气体,正反应放热
C.AB为气体,A2、B2中最少有一种为非气体,正反应吸热
D.AB为固体,A2、B2中最少有一种为非气体,正反应吸热
参考答案:B???
本题解析:温度由500℃到300℃时,AB%增加平衡正向移动,即正反应放热;在t3时加压,AB%减小,平衡逆向移动,即逆向气体体积缩小。
本题难度:一般
5、选择题 做导电实验,灯泡很暗
B.0.1mol・L-1HR溶液稀释到100倍时,溶液的pH值为3.1
C.20mL0.1mol・L-1HR恰好中和20mL0.1mol・L-1NaOH溶液
D.0.1mol・L-1NH4R溶液的pH等于7
参考答案:BD
本题解析:
【错解分析】由于思维定势,灯泡较暗,对应的电解质就是弱电解质。这里忽略了一个重要的条件,即在相同条件(主要是浓度)下。如果没有这个前提,用0.1mol・L-1的HAc溶液和1×10-4mol・L-1HCl作导电实验,醋酸溶液中氢离子的浓度大约为13.2×10-4mol・L-1,而盐酸溶液中去离子的浓度只有1×10-4mol・L-1,很明显前者的导电能力比后者强。因此A的错误选项,它不能说明HR是弱电解质。
选项C提供的中和反应的事实,不能说明酸的强弱。中和反应只说明酸、碱提供的氢离子和氢氧根
本题难度:简单