微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有可逆反应Fe(s)+CO2(g)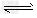 FeO(s)?+?CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2?。
FeO(s)?+?CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2?。
(1)能判断该反应达到平衡状态的依据是___________(填序号)。 ?????
A.容器内压强不变了???????????
B.c(CO)不变了 ?????
C.v正(CO2)=v逆(CO)??????
D.c(CO2)=c(CO)
(2)该反应的正反应是_______(选填“吸热”、“放热”)反应。
(3)写出该反应的平衡常数表达式__________。若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.0mol/L,某温度时达到平衡,此时容器中CO的浓度为1.0?mol/L,则该温度下上述反应的平衡常数K=__________(保留二位有效数字)。
(4)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,反应混合气体中CO2的物质的量分数如何变化(选填“增大”、“减小”、“不变”)。 ????
①升高温度__________;②再通入CO___________。
(5)该反应的逆反应速率随时间变化的关系如下图:
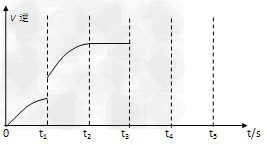
①从图中看到,反应在t2时达平衡,?在t1时改变了某种条件,改变的条件可能是______________________。 ?????
A.升温???????B.增大CO2浓度 C.使用催化剂
②如果在t3时从混合物中分离出部分CO,t4~?t5时间段反应处于新平衡状态,请在图上画出t3~?t5的V(逆)变化曲线。
参考答案:(1)BC
(2)吸热
(3)k=c(CO)/c
本题解析:
本题难度:一般
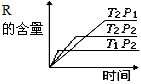
2、选择题 在密闭容器中进行下列反应:M (g)+N (g) R (g)+2 L 此反应符合下面图像。下列叙述正确的是
R (g)+2 L 此反应符合下面图像。下列叙述正确的是
 [???? ]
[???? ]
A.正反应吸热,L是气体
B.正反应吸热,L是固体
C.正反应放热,L是液体
D.正反应放热,L是气体
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列说法中正确的是
[???? ]
A.在一体积不变的密闭容器中,反应2NO2(g)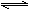 N2O4(g) ΔH<0,达平衡后加热,容器内气体的平均摩尔质量减小,但气体的密度不变
N2O4(g) ΔH<0,达平衡后加热,容器内气体的平均摩尔质量减小,但气体的密度不变
B.在一体积和温度不变的容器中,进行反应H2(g)+I2(g)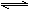 2HI(g) ΔH<0,若容器内的压强不变,表明反应已达平衡状态,且反应从开始至达到平衡状态的过程中,容器向外放热
2HI(g) ΔH<0,若容器内的压强不变,表明反应已达平衡状态,且反应从开始至达到平衡状态的过程中,容器向外放热
C.在一温度和压强不变的密闭容器中,充入一定量的SO3发生反应2SO3 (g)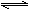 2SO2(g)+O2(g),达平衡后,再向容器中充入一定量的SO3,重新达到平衡时,SO3的体积分数增加
2SO2(g)+O2(g),达平衡后,再向容器中充入一定量的SO3,重新达到平衡时,SO3的体积分数增加
D.四个体积相等的密闭容器,四位同学分别于不同的温度下,按物质的量1:3的比例在其中分别充入等量的N2和H2合成氨,当反应进行到10分钟时,每人均测定各自四个容器中NH3的体积分数并分别作图如下,则图2肯定错误 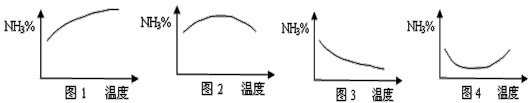
参考答案:A
本题解析:
本题难度:一般
4、填空题 Ⅰ.如下图所示,将2molA气体和1molB气体充入一容积可变的密闭容器中,发生反应:2A(g)+B(g) 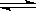 2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为 ;该条件下的反应的平衡常数为 。
2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为 ;该条件下的反应的平衡常数为 。

Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的热化学方程式 。
(2)利用该反应可设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式 。
(3)用石墨做阳极,铁棒做阴极,电解硫酸铜溶液,则石墨棒上的电极反应式为 ;如果起始时盛有1000mL PH=5的硫酸铜溶液(25℃)(足量),一段时间后溶液的PH变为1,若要使溶液恢复到起始浓度(忽略溶液体积变化),可向溶液中加入 (填物质名称),其质量约为 。
参考答案:Ⅰ. 90%(2分) 56
本题解析:略
本题难度:困难
5、选择题 下图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)

A.等于1.369 g・L-1
B.等于2.054 g・L-1
C.在1.369g・L-1和2.054g・L-1之间
D.在2.054g・L-1和4.108g・L-1之间
参考答案:D
本题解析:
试题分析:NO与氧气恰好符合物质的量之比是2:1的关系,所以二者恰好完全反应生成NO2,若全部是二氧化氮,则恒压下气体的密度即为二氧化氮在标准状况下的密度46g/22.4L=2.054g/L,但二氧化氮存在
如下平衡2NO2 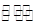 N2O4 ,若二氧化氮全部转化为N2O4,恒压下气体的密度是N2O4的密度为92g/22.4L=4.108g/L,而实际的气体的密度应介于二者之间,所以答案选D。
N2O4 ,若二氧化氮全部转化为N2O4,恒压下气体的密度是N2O4的密度为92g/22.4L=4.108g/L,而实际的气体的密度应介于二者之间,所以答案选D。
考点:考查混合气体密度的判断,极端假设法的应用
本题难度:一般