微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在2L密闭容器中,800℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5
n(NO)/mol
0.020
0.010
0.008
0.007
0.007
0.007
(1)写出该反应的平衡常数表达式:K=______,已知:K(300℃)>K(350℃),该反应是______反应(填“放热”或“吸热”).
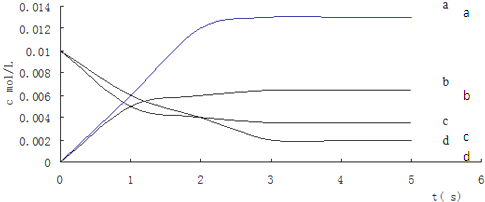
(2)图中表示NO2的变化的曲线是______,用O2的浓度变化表示从0~2s内该反应的平均速率v=______.
(3)能说明该反应已经达到平衡状态的是______
a.v(NO2)=2v(O2)????????????????b.容器内压强保持不变
c.v逆(NO)=2v正(O2)?????????????d.容器内物质的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是______
a.及时分离出NO2气体??????????????? b.适当升高温度
c.增大O2的浓度???????????????????? d.选择高效的催化剂.
2、简答题 研究NO2、SO2、CO等大气污染气体的处理有重要意义.
(1)NO2可用水吸收,相应的化学方程式为______.利用反应
6NO2+8NH3 催化剂
△
7N2+12H2O也可以处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是______L.
(2)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1
则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=______kJ?mol-1
一定条件下,将与体积比1:2置于密闭容器中发生上述反应,下列能说明反映达到平衡状态的是______.
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d.每消耗1molSO3的同时生成1molNO2
测得上述反应平衡时的NO2与SO2体积比为1:6,则平衡常数K=______.
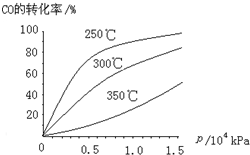
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应△H______0(填“>”或“<”).实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是______.
3、选择题 某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是
|
网站客服QQ: 960335752 - 14613519 - 791315772