微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 选做(1)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据)。根据下图回答下列问题:

(a)P和Cl2反应生成PCl3的热化学方程式是______________________________ ;
(b)P和Cl2分两步反应生成1 mol PCl5的ΔH3=____________________,P和Cl2一步反应生成1 mol PCl5的ΔH4____________ΔH3(填“大于”.“小于”.或“等于”)。
(2)在微生物作用的条件下,NH经过两步反应被氧化成NO。这两步的能量变化示意图如下:
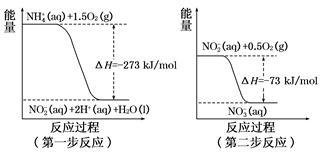
(a)第二步反应是________反应(选填“放热”或“吸热”),判断依据是__________ 。
(b)1molNH4+(aq)全部氧化成NO2-(aq)的热化学方程式是_____________________________________。
参考答案:(1)(a) 本题解析:
本题解析:
试题分析:(1)(a)根据反应过程和能量关系图,得出:P(s)+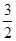 Cl2(g)=PCl3(g)△H=-306kJ・mol-1;(b)P(s)+
Cl2(g)=PCl3(g)△H=-306kJ・mol-1;(b)P(s)+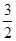 Cl2(g)=PCl3(g)△H1①,PCl3(g)+Cl2(g)=PCl3(g)△H2 ②,①+②得:P(s)+
Cl2(g)=PCl3(g)△H1①,PCl3(g)+Cl2(g)=PCl3(g)△H2 ②,①+②得:P(s)+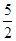 Cl2(g)=PCl5(g)△H3=△H1+△H2=-306-93kJ・mol-1=-399kJ・mol-1;根据盖斯定律,只要是始态和终态不变,无论是一步还是多步完成,反应热不变,填写“等于”;(2)(a)一个反应是放热反应还是吸热反应,决定于反应物的总能量与生成物的的总能量的相对大小,反应物的总能量大于生成物的总能量,此反应是放热反应,△H<0,如果反应物的总能量小于生成物的总能量,此反应是吸热反应,△H>0,根据图中信息,反应物的总能量大于生成物的总量,是放热反应,依据是:△H<0或者反应物的总能量大于生成物的总能量;(b)根据第一步反应的图,热化学反应方程式:NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H=-273kJ・mol-1。
Cl2(g)=PCl5(g)△H3=△H1+△H2=-306-93kJ・mol-1=-399kJ・mol-1;根据盖斯定律,只要是始态和终态不变,无论是一步还是多步完成,反应热不变,填写“等于”;(2)(a)一个反应是放热反应还是吸热反应,决定于反应物的总能量与生成物的的总能量的相对大小,反应物的总能量大于生成物的总能量,此反应是放热反应,△H<0,如果反应物的总能量小于生成物的总能量,此反应是吸热反应,△H>0,根据图中信息,反应物的总能量大于生成物的总量,是放热反应,依据是:△H<0或者反应物的总能量大于生成物的总能量;(b)根据第一步反应的图,热化学反应方程式:NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H=-273kJ・mol-1。
考点:考查反应热、热化学反应方程式的书写等相关知识。
本题难度:困难
2、选择题 下列叙述正确的是?????????????????????????????????? ( )
A.分子晶体中的每个分子内一定含有极性共价键
B.原子晶体中的相邻原子间只存在非极性共价键
C.含有阴离子的化合物一定含有阳离子
D.金属晶体的熔点和沸点都很高
参考答案:C
本题解析:稀有气体元素最外层电子已经达到稳定结构,其单质分子内不存在化学键。构成原子晶体的元素不一定都是同一种元素,也可以存在极性键。金属晶体的熔沸点有的很低,例如碱金属等。所以正确的答案是C。
本题难度:一般
3、选择题 化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是
A.该合成中所有的电能和热能全部转化为化学能
B.该合成氨过程不属于氮的固定
C.空气、水、太阳能均为可再生资源
D.断裂N2中的N≡N键会释放出能量
参考答案:C
本题解析:
试题分析:A、在用空气和水作原料合成氨气的过程中,能量的利用率不可能是100%,所以电能和热能不可能全部转化为化学能,错误;B、氮的固定是把游离态氮转化为化合态氮的过程,空气中氮气是游离态,氨气中氮是化合态,属于氮的固定,错误;C、空气、水、太阳能都属于再生能源,正确;D、化学键的断裂需要吸收能量,错误,答案选C。
考点:考查对能量的利用、物质的转化的判断
本题难度:一般
4、填空题 甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃.
(1)甲硅烷中含有的化学键是______,其在固态时属于______晶体.
(2)已知室温下1g甲硅烷自燃生成SiO2和液态水放出热量44.6kJ,则其热化学方程式为______.
参考答案:(1)SiH4由非金属形成的化合物,非金属元素之间的化学键为
本题解析:
本题难度:一般
5、选择题 下列离子方程式书写正确的是(???)
A.氢硫酸与过量氢氧化钠溶液反应H++OH-====H2O
B.稀硫酸与氢氧化钡溶液反应H++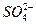 +Ba2++OH-====BaSO4↓+H2O
+Ba2++OH-====BaSO4↓+H2O
C.硫酸铜溶液与硫化钾溶液混合反应Cu2"++S2-====CuS↓
D.氯化铵固体与消石灰混合加热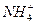 +OH-====NH3↑+H2O
+OH-====NH3↑+H2O
参考答案:C
本题解析:A中氢硫酸是难电离的物质,不能拆写成离子符号,应该保留化学式;B中化学计量数只进行了部分约简,改变了反应的物质的量之比,正确书写应为:2H++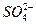 +Ba2++2OH-====BaSO4↓+2H2O;D中反应物都是固体,不能写离子方程式,只能写反应的化学方程式。
+Ba2++2OH-====BaSO4↓+2H2O;D中反应物都是固体,不能写离子方程式,只能写反应的化学方程式。
本题难度:一般