微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.蓄电池充电时其负极应与外电源的的正极相连接
B.同温同压下,H2(g)+Cl2(g)==2HCl(g)在光照和点燃条件下的△H相同
C.已知:H2(g)+I2(g)  2HI(g);△H =-9.48 kJ/mol,若将254g I2(g)和2gH2(g)充分反应可放出9.48 kJ的热量
2HI(g);△H =-9.48 kJ/mol,若将254g I2(g)和2gH2(g)充分反应可放出9.48 kJ的热量
D.已知在101 kPa时,2 g碳燃烧生成CO放出热量为Q kJ,则碳的燃烧热为6Q kJ・mol-1
2、填空题 (10分,每空2分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水,将这二种物质混合时可发生如下反应:N2H4+2 H2O2 N2+4H2O,已知0.4 mol液态肼和足量的液态双氧水反应,生成氮气和水蒸汽,放出256.6kJ的热量。
N2+4H2O,已知0.4 mol液态肼和足量的液态双氧水反应,生成氮气和水蒸汽,放出256.6kJ的热量。
(1)反应的热化学方程式为_________________________________________________。
(2)又已知:H2O(l) H2O(g);ΔH="+44" kJ/mol。则16 g液态肼和足量的液态双氧水反应生成液态水时放出的热量是_______________kJ。
H2O(g);ΔH="+44" kJ/mol。则16 g液态肼和足量的液态双氧水反应生成液态水时放出的热量是_______________kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有很大的优点是
(4)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计
成原电池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应为
3、选择题 在C(HCO3-)=0.1mol?L-1的溶液中,可以大量共存的离子组是
A.Ca2+、NO3-、NH4+、Cl-
B.Na+、SO42-、C1-、Ca2+
C.H+、Ba2+、Cl-、NO3-
D.Cl-、CO32-、Na+、OH-
4、填空题 (9分)如图所示,在一个小烧杯里加入研细的20g Ba(OH)2・8H2O晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入10g NH4CL晶体,并用玻璃棒快速搅拌。
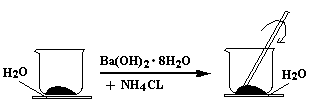
(1)实验中要用玻璃棒搅拌的原因是 。
(2)写出该反应的化学方程式 。
该反应 (填“是”或“不是”)氧化还原反应。
(3)该实验的现象有 。
(4)该反应为 (填“吸”或“放”)热反应,这是由于反应物的总能量 (填“大于”或“小于”)生成物的总能量。
5、选择题 等体积等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合,离子方程式正确的是
A.HCO3-+OH-→H2O+C
B.2HCO3-+Ba(OH)2→BaCO3↓+2H2O+C
C.HCO3-+Ba2++OH-→H2O+BaCO3↓
D.2HCO3-+Ba2++2OH-→BaCO3↓+2H2O+C