微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在无色透明溶液中,能够大量共存的离子组是
A.I-、ClO-、K+、H+
B.Na+、Cu2+、Cl-、SO42-
C.H+、Ca2+、Cl-、CO32-
D.Na+、Cl-、NO3-、CO32-
参考答案:D
本题解析:分析:溶液无色透明,则有颜色的离子不能大量存在,如离子之间不发生任何反应,则可大量共存.
解答:A.溶液无色,但ClO-与H+生成弱电解质HClO而不能大量共存,且ClO-与I-发生氧化还原反应,故A错误;
B.Cu2+有颜色,不符合题意,故B错误;
C.CO32-与H+反应生成二氧化碳气体而不能共存,且CO32-与Ca2+反应沉淀,故C错误;
D.四种离子无色,且离子之间不发生任何反应,能大量存在,故D正确.
故选D.
点评:本题考查离子共存问题,题目难度不大,本题注意常见有颜色的离子的种类,注意离子反应的类型以及离子的性质.
本题难度:简单
2、选择题 能大量共存于同一溶液,加入NaOH溶液也没有新的离子反应发生的是
A.Na+、K+、SO42-、[Al(OH)4]-
B.Fe3+、Ca2+、I-、NO3-
C.K+、NH4+、SO42-、Br-
D.Mg2+、Ca2+、HCO3-、Cl-
参考答案:A
本题解析:分析:能大量共存于同一溶液,说明离子之间不发生任何反应,加入NaOH溶液也没有新的离子反应发生,说明离子与OH-不发生反应,以此解答该题.
解答:A.离子之间不发生任何反应,且与OH-不发生反应,可大量共存,故A正确;
B.Fe3+、NO3-与I-因发生氧化还原反应而不能大量共存,加入NaOH,Fe3+与OH-反应生产沉淀,故B错误;
C.离子能大量共存,加入NaOH溶液,NH4+与OH-反应,故C错误;
D.加入NaOH溶液,Mg2+、HCO3-都能与OH-反应,分别生产氢氧化镁和碳酸钙沉淀,故D错误.
故选A.
点评:本题考查离子共存问题,综合考查学生化学知识的应用能力,为高考常见题型,注意把握常见离子的性质,把握提给信息,为解答该题的关键,注意题中加入NaOH溶液反应的要求,为易错点,题目难度中等.
本题难度:一般
3、选择题 已知破坏1 mol H―H键、Cl―Cl键、H―Cl键分别需要吸收436kJ、243kJ、432kJ能量,则由H2与CL2生成1 mol HCL总的过程需要 ( )
A.放热185kJ
B.吸热185kJ
C.放热92.5kJ
D.吸热92.5kJ
参考答案:C
本题解析:略
本题难度:简单
4、填空题 (17分)针对化学反应中的能量变化解决下列问题。
(1)测定稀硫酸和稀氢氧化钠中和热(中和热为57.3 kJ・mol-1)的实验装置如图所示。某兴趣小组的实验数值结果小于57.3 kJ・mol-1,原因可能是 (填字母)。
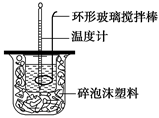
a.实验装置保温、隔热效果差
b.读取混合液的最高温度记为终点温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度
(2)今有如下两个热化学方程式:则a b(填“>”、“=”或“<”)。
H2(g)+1/2O2(g)=H2O(g) ΔH1=a kJ・mol-1
H2(g)+1/2O2(g)=H2O(l) ΔH2=b kJ・mol-1
参考答案:
本题解析:
本题难度:一般
5、选择题 下列反应既属氧化还原反应,又属放热反应的是(?? )
A.铝片与稀盐酸的反应
B.Ba(OH)2・8H2O与NH4Cl的反应
C.灼热的碳与二氧化碳的反应
D.甲烷在氧气中的燃烧反应
参考答案:AD
本题解析:A、C、D属氧化还原反应,B为复分解反应属非氧化还原反应,A、D属放热反应,而灼热碳与二氧化碳的反应是吸热反应。
本题难度:一般