微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子在溶液中因发生氧化还原反应而不能大量共存的是( ???)
A.H??+、NO3-、Fe2+、Na+
B.Ag+、NO3-、Cl-、K+
C.K+、Ba2+、OH-、SO42-
D.Cu2+、NH4+、Br-、OH-
参考答案:A
本题解析:试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A中溶液显酸性,在酸性条件下,NO3-能氧化Fe2+,不能大量共存;B中生成氯化银沉淀,不是氧化还原反应;C中生成硫酸钡白色沉淀,但不是氧化还原反应;D中Cu2+、NH4+与OH-均反应。不能大量共存,但反应不是氧化还原反应,答案选A。
考点:考查离子共存的正误判断
点评:该题是高考中的高频题,属于中等难度的试题,试题侧重考查学生的能力。该题需要明确离子不能大量共存的一般情况,即(1)能发生复分解反应的离子之间;(2)能生成难溶物的离子之间;(3)能发生氧化还原反应的离子之间;(4)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有:(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。
本题难度:一般
2、实验题 某小组查文献得知:氧化性I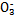 >Fe3+>I2,3Br2+6FeCl2
>Fe3+>I2,3Br2+6FeCl2 2FeBr3+4FeCl3;I2+2S2
2FeBr3+4FeCl3;I2+2S2
 S4
S4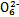 +2I-;CuI是一种白色沉淀(Ksp=1.3×1
+2I-;CuI是一种白色沉淀(Ksp=1.3×1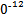 )。
)。
Ⅰ.该小组为确定一份加碘盐(可能含有KIO3、KI、Mg2+、Fe3+)的成分,设计定性实验加以猜想和验证。
(1)实验过程如下:
实验步骤
| 实验过程和现象
| 对应结论
|
步骤1
| 取一定量碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得试液分为3份
| ?
_____________
|
?
步
骤
2
| 第①份
试液
| 
| 碘盐中肯定含 ?
|
第②份
试液
| 
| ?
_____________
|
第③份
试液
| 
| X为 (填化学式)?
?
(2)该碘盐中肯定不含的物质是 (用化学式或离子符号表达)。?
(3)根据信息推断Fe3+、S4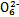 、I2、Br2的氧化性由强到弱的顺序是 。? 、I2、Br2的氧化性由强到弱的顺序是 。?
(4)第③份试液中加入足量KI固体后,反应的离子方程式为 、 。?
Ⅱ.用“间接碘量法”测定含有CuCl2・2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:
取0.40 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。加入淀粉作滴定指示剂,用0.100 0 mol・L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
(1)滴定终点的现象是 。?
(2)CuCl2溶液与KI反应的化学方程式为 。?
(3)该试样中CuCl2・2H2O的质量分数为 。?
参考答案:Ⅰ.(1)Fe3+ CCl4 (2)KI
(3)Br2
本题解析:Ⅰ.(2)由步骤②③可知溶液中一定不含KI,结合加碘食盐可知一定含有KIO3;(4)溶液中的Fe3+、I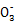 均与I-反应;Ⅱ.依据2CuCl2+4KI 均与I-反应;Ⅱ.依据2CuCl2+4KI 本题难度:一般 本题难度:一般
3、选择题 二氧化碳与NaOH溶液反应生成的盐是
A.只能生成碳酸钠
B.只能生成碳酸氢钠
C.生成不溶于水的沉淀
D.可能是碳酸钠和碳酸氢钠的混合物
参考答案:D
本题解析:如果CO2和NaOH两者反应量不同,可能产生不同产物.
本题难度:一般
4、填空题 (8分)现有三种物质A、B、C,它们均溶于水。其中有一种是酸,一种是碱,一种是盐,溶于水后电离,可以产生下表中的离子:
阳离子
| Na+???H+?????Ba2+
| 阴离子
| OH-?? CO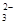 ??? SO ??? SO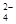 ? ?
为鉴别它们,分别完成以下实验,其结果如下:
① A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
② B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝 酸。 酸。
请根据上述实验结果,填空:
(1)写出下列物质的化学式:X??????????????????
(2)B溶于水后的电离方程式为??????????????????????????????????????
(3)鉴别B中阴离子的实验操作方法是??????????????????????????????
(4)B与C反应的离子方程式:??????????????????????????
参考答案:
 本题解析:略 本题解析:略
本题难度:一般
5、选择题 下列可以大量共存且溶液是无色的离子组是
A.Fe3+、Na+、Cl─、SO42─
B.Ba2+、Fe2+、Cl─、SO42─
C.NO3-、SO42-、K+、Mg2+
D.H+、K+、OH-、NO3─
参考答案:C
本题解析:分析:溶液无色,则有颜色的Fe2+、Fe3+离子不符合题意,其它溶液无色,根据离子之间是否发生反应生成沉淀、气体、水或氧化还原反应时判断离子能否大量共存.
解答:A、Fe3+离子呈黄色,与溶液无色不符,故A错误;
B、Fe2+离子呈浅绿色,与溶液无色不符,且钡离子与硫酸根离子反应生成沉淀,不能共存,故B错误;
C、选项中四种离子不发生任何反应,可以大量共存,故C正确;
D、H+离子与OH-离子发生中和反 应而不能大量共存,故D错误.
故选C.
点评:本题考查离子共存,题目难度不大,本题注意溶液无色的要求,根据离子之间能否反应判断离子共存问题.
本题难度:困难
|
|