��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����Һ�������25�棬�й������У���ȷ����
A��ij��Һ��ˮ�������c(H��)=10-13�������Һ��pHһ��Ϊ13
B��pH��4.5�ķ���֭��c(H��)��pH��6.5��ţ����c(H��)��2��
C��Ũ����ͬ�İ�ˮ������������ϣ�������ҺpH=7
D��pH��7��CH3COOH��CH3COONa�����Һ�У�c(Na��)=c(CH3COO��)
�ο��𰸣�D
�����������Һ��ˮ�������c(H��)=10-13�������Һ��ˮ�ĵ����DZ����Ƶģ�������Һ���������ԣ�Ҳ�����Լ��ԣ�A����ȷ��pH��4.5��pH��6.5����Һ��c(H��)�ֱ���10��4.5��10��6.5�����Զ��ߵ�������Ũ��֮����100�U1��B����ȷ��һˮ�ϰ���������ʣ�������ǡ�÷�Ӧʱ�����ɵ��Ȼ��ˮ�⣬��Һ�����ԣ�C����ȷ��ѡ��D�и��ݵ���غ��֪c(H��)��c(Na��)=c(CH3COO��)��c(OH��)�����pH��7����c(H��)=cc(OH��)������c(Na��)=c(CH3COO��)��D��ȷ����ѡD��
�����Ѷȣ���
2��ѡ���� �֣�ÿ��CO��CH4��Ϊ�����Ŀ�ȼ�����塣
��1���������CO��CH4����ͬ�����·ֱ���ȫȼ�գ�ת�Ƶĵ�����֮����
��2����֪��101kPaʱ��CO��ȼ����Ϊ283kJ/mol����ͬ�����£���2 molCH4��ȫȼ������Һ̬ˮ�����ų�������Ϊ1 mol CO��ȫȼ�շų�������6.30����CH4��ȫȼ�շ�Ӧ���Ȼ�ѧ����ʽ�� ��
��3��120�桢101kPa�£�a mL��CO��CH4��ɵĻ��������b mLO2����ȫȼ�պָ���ԭ�¶Ⱥ�ѹǿ��
�������������O2ǡ����ȫ��Ӧ������bmL CO2������������CH4���������Ϊ
������2λС������
����ȼ�պ����������С��a/4mL����a��b��ϵ����ѧ����ʽ�� ��
�ο��𰸣���1��1��4
��2��CH4(g)��2O2(g)��CO2
�����������
�����Ѷȣ�һ��
3��ѡ���� 25�棬101 kPaʱ��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ���к���Ϊ57.3kJ��mol-1�������ȼ����Ϊ
5518 kJ��mol-1�������Ȼ�ѧ����ʽ��д��ȷ���� [???? ]
A.2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq) =BaSO4(s)+2H2O(l), ��H=-114.6 kJ��mol-1
B.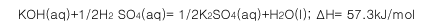
C. C8H8(l)+25/2O2(g)==8CO2+9H2O,��H=-5518kJ/mol
D.2C8H18(g) +25O2(g) =16CO2(g) + 18H2O(l), ��H = -5518 kJ��mol-1
�ο��𰸣�B
���������
�����Ѷȣ���
4��ѡ���� ����Һ�������25�棬�����й�������ȷ����(???? )
A��PHֵ��ͬ��������Ȼ����Һ��ˮ�ĵ���̶���ͬ
B��ij��Һ����ˮ�������c(H+)=10-13,�����Һ��PHһ��Ϊ13
C��PH=4.5�ķ���֭��c(H+)��PH=6.5��ţ����c(H+)��2��
D���к�Ũ�Ⱥ��������ͬ������ʹ��ᣬ���ĵ��������Ƶ����ʵ���֮��Ϊ1��1
�ο��𰸣�D
���������
���������A����������ˮ�ĵ��룬�Ȼ��ˮ��ٽ�ˮ�ĵ��룬PHֵ��ͬ��������Ȼ����Һ��ˮ�ĵ���̶�ǰ��С�ں��ߣ�����B��ij��Һ����ˮ�������c(H+)=10-13��˵��ˮ�ĵ����ܵ����ƣ�������������ˮ�ĵ��룬�����Һ��PH����Ϊ1��13������C��PH=4.5�ķ���֭��c(H+)��PH=6.5��ţ����c(H+)��100����D��Ũ�Ⱥ��������ͬ������ʹ��������ʵ����ʵ�����ͬ���к�Ũ�Ⱥ��������ͬ������ʹ��ᣬ���ĵ��������Ƶ����ʵ���֮��Ϊ1��1����ȷ��
�����Ѷȣ�һ��
5��ѡ���� �ڲ�ͬ�¶��£�ˮ�ﵽ����ƽ��ʱc��H+����c��OH�����Ĺ�ϵ��ͼ4��ʾ������˵������ȷ����
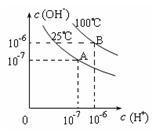
A��100��ʱ��pH=12��NaOH��Һ��pH=2��H2SO4��Һǡ���кͣ�������Һ��pH����7
B��25��ʱ,0.2 mol/L Ba(OH)2��Һ��0.2 mol/L HCl��Һ�������ϣ�������Һ��pH����7
C��25��ʱ, 0.2 mol/L NaOH��Һ��0.2 mol/L������Һǡ���кͣ�������Һ��pH����7
D��25��ʱ,pH=12�İ�ˮ��pH=2��H2SO4��Һ�������ϣ�������Һ��pH����7
�ο��𰸣�D
���������
���������100��ʱ��pH=12��NaOH��ҺŨ����1mol/L�����Է�Ӧ�����������ǹ����ģ���Һ�Լ��ԣ�A����ȷ��B�����������ǹ����ģ���Һ�Լ��ԣ�B����ȷ��C��ǡ�÷�Ӧ�������ɵĴ�����ˮ�⣬��Һ�Լ��ԣ�C����ȷ��D�а�ˮ��������Һ�Լ��ԣ�D��ȷ����ѡD��
������������Һ��ѡA����������û�п��ǵ�ˮ�����ӻ����������¶ȵ����߶�����ģ������100��ʱ��pH��6ʱ����Һ�������Եġ����������pH�ж���Һ�����ʱ����Ҫע����Һ���¶ȡ�
�����Ѷȣ�һ��