��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� (12��)ijͬѧΪ��̽��п�����ᷴӦ�����е����ʱ仯������100mLϡ�����м���������п�ۣ����������ˮ�������ռ���Ӧ�ų���������ʵ���¼����(�ۼ�ֵ)��
ʱ��(min)
| 1
| 2
| 3
| 4
| 5
|
�������(mL)(��״��)
| 50
| 120
| 232
| 290
| 310
(1)��һʱ���(ָ0��1��1��2��2��3��3��4��4��5min)��Ӧ�������______________��ԭ����______________________________________________��
(2)��һʱ��εķ�Ӧ������С________________��ԭ����___________________��
(3)��2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����(����Һ������䣬Ҫд���������)______________________________________________________��
(4)��ͬѧ����ϡ������п��ȡ������ʵ���У����ּ�����������ͭ��Һ�ɼӿ��������������ʡ���ش��������⣺
������ʵ�����漰�������ӷ�Ӧ����ʽ��
��
������ͭ��Һ���Լӿ������������ʵ�ԭ���� ��
��ʵ����������Na2SO4��MgSO4��Ag2SO4��K2SO4��4����Һ������ʵ����CuSO4 ��Һ���������õ��� ��
�ܸ�ͬѧͨ��ʵ���һ���о�������ͭ�����������������ʵ�Ӱ�졣��ͬѧ���ó��Ľ���Ϊ������������CuSO4��Һʱ���������������ʻ�����ߡ����������CuSO4��Һ����һ����ʱ���������������ʷ������½���������������������½�����Ҫԭ��
��
2��ѡ���� ���ڷ�ӦA+3B�T2C+D��˵�����з�Ӧ�����������ǣ�������
A��v��A��=0.1mol/��L?min��
B��v��B��=0.6mol/��L?min��
C��v��C��=0.5mol/��L?min��
D��v��D��=0.3mol/��L?min��
3������� ��һ���¶��£���֪�ڸ��¶��£��������������ʾ�Ϊ��̬����10 L�ܱ������м���5 mol SO2.4 mol O2����10 min��Ӧ��ƽ��ʱ��2 mol SO2�����˷�Ӧ���Լ��㣺
��1����SO2��ʾ�÷�Ӧ�ķ�Ӧ���ʣ�
��2��O2��ת���ʣ�
��3�����¶��µ�ƽ�ⳣ��K��������λ��Ч���֣���
4��ѡ���� һ���¶��£���2L���ܱ������з������·�Ӧ�� B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼl����ƽ����� B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼl����ƽ����� ʱ��ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2�������й�˵����ȷ���� ʱ��ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2�������й�˵����ȷ����
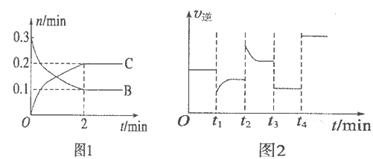
A��x=2����Ӧ��ʼ2 min��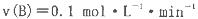
B��t1ʱ�ǽ��£�ƽ�������ƶ�
C��t2ʱ�ı����������������c(C����ƽ��ʱB�����ʵ�����������
D��t3ʱ�����Ǽ�Сѹǿ��ƽ�ⲻ�ƶ���t4ʱ������ʹ�ô�����c (B)����
5��ʵ���� Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ��ͨ�����ڵ��ں� pH��Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø� ���������л���Ⱦ��p-CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�졣
ʵ����ơ�
����p-CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298 K��313 K(����ʵ���������±�)��������¶Ա�ʵ�顣
(1)���������ʵ����Ʊ�(���в�Ҫ���ո�)��
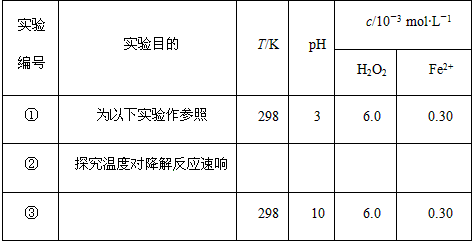
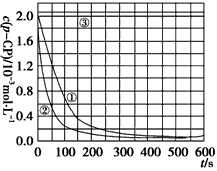
���ݴ�����
ʵ����p-CP��Ũ����ʱ��仯�Ĺ�ϵ����ͼ��
(2)�������ͼʵ������ߣ����㽵�ⷴӦ50��150 s�ڵķ�Ӧ���ʣ� v(p-CP)��________mol��L-1��s-1�����������
(3)ʵ��١��ڱ����¶����ߣ����ⷴӦ���������¶ȹ���ʱ�������½��ⷴӦ���ʼ�С�����Fenton�������Լ�H2O2�ĽǶȷ���ԭ��________________________________________________________________________��
(4)ʵ��۵ó��Ľ����ǣ�pH����10ʱ��_______________________________��˼���뽻��
(5)ʵ��ʱ���ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�еķ�Ӧ����ֹͣ������������ͼ�е���Ϣ������һ��Ѹ��ֹͣ��Ӧ�ķ�����________��
|