��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (8��)��T��ʱ��ˮ�����ӻ�ΪKW��10��12���ڴ��¶��£���pH��a��������ҺVa L��pH��b��Ba(OH)2��ҺVb L��ϣ�
(1)�����ݿ����ж�T???????????25(����ڡ� ����С�ڡ��������ڡ�)�������ǣ�???????????????????????????????????????????????????????��
��2�������û��ҺΪ���ԣ���a��b��10����Va�UVbΪ???????????��
��3�������û��Һ��pH��10����a��2��b��12��Va�UVbΪ???????????��
�ο��𰸣�(1)���ڣ�ˮ�ĵ��������ȹ��̣��¶����ߣ�ˮ�ĵ���ƽ�����ƣ�
���������ˮ�ĵ�������Ǹ����ȹ���,�ڳ���ʱˮ�����ӻ�ΪKW��10��14,�ȳ���ʱ�����ӻ�Ҫ��,˵���¶ȱȳ���ʱ�ĸߣ������¶Ȳ�ͬ��Ӧ�����µ����������й���ҺpH����ؼ��㡣
�����Һ������,����10-a.Va=10(b-12).VB ��������û����Һ��pH=10,��˵����Ϻ���Һ�ʼ���,�����,����10(b-12).Vb-10-a.Va=(Va+Vb).10(10-12)
�����Ѷȣ�һ��
2������� ����һ�������£���ѧ�����ô��̵����з����CO2��̫���ܵ�ص��ˮ������H2�ϳɼ״������������ͼ��ʾ���Իش��������⣺

��1���úϳ�·�߶��ڻ��������ļ�ֵ���� ��
��2��15��20%���Ҵ�����HOCH2CH2NH2��ˮ��Һ���������ԣ������ϳ���·������CO2���ռ��������ӷ���ʽ��ʾ�Ҵ���ˮ��Һ�������Ե�ԭ�� ��
��3��CH3OH��H2��ȼ���ȷֱ�Ϊ����H����725.5 kJ/mol����H����285.8 kJ/mol��д����ҵ����CO2��H2�ϳ�CH3OH���Ȼ�ѧ����ʽ�� ��
��ȼú�����е�CO2ת��Ϊ���ѵķ�Ӧԭ��Ϊ��
2CO2(g) + 6H2(g)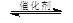 CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)
��֪һ��ѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ת���ʼ��±���
Ͷ�ϱ�[n(H2) / n(CO2)]
| 500 K
| 600 K
| 700 K
| 800 K
|
1.5
| 45%
| 33%
| 20%
| 12%
|
2.0
| 60%
| 43%
| 28%
| 15%
|
3.0
| 83%
| 62%
| 37%
| 22%
��4���÷�Ӧ���ʱ��H 0���ر��S 0�����������
��5���ü�����Ϊȼ�ϵ��ԭ�ϣ��ڼ��Խ����иõ�ظ����ĵ缫��Ӧʽ ��
��6������1.12 L��min-1����״������������õ����ͨ����ѣ��е�Ϊ-24.9 �棩���øõ�ص��500 mL 2 mol��L-1 CuSO4��Һ��ͨ��0.50 min�������Ͽ���������ͭ g��
�ο��𰸣���1�������ڷ�ֹ����ЧӦ ��2�֣�
��2��HOCH2C
���������
�����������1�������������̼�ϳɼ״��������˶�����̼���ŷţ������ڷ�ֹ����ЧӦ
��2��HOCH2CH2NH2ˮ��ʹ��Һ�ʼ��ԣ����������ӷ���ʽΪHOCH2CH2NH2+H2O HOCH2CH2NH3++OH- HOCH2CH2NH3++OH-
��3�����ݸ�˹���ɣ����״���������ȼ���Ȼ�ѧ����ʽ����Ӧ�������á�H=��285.8 kJ/mol��3-(��725.5 kJ/mol)=-131.9kJ/mol,���Ժϳɼ״����Ȼ�ѧ����ʽΪCO2(g)+3 H2(g)= CH3 OH(l)+ H2O(l) ��H=-131.9kJ/mol
��4�����¶����ߣ�������̼��ת���ʽ��ͣ�˵������ƽ���������ƶ�������Ӧ����Ϊ���ȷ�Ӧ����H<0����Ӧ������������ʵ�����8mol������������������ʵ�����4mol�����ԡ�S<0��
��5���õ�ظ����Ǽ��ѷ���������Ӧ�����Խ���������̼������ӣ��缫��ӦʽΪCH3 OCH3 -12e-+16 OH-=2CO32-+11 H2O
��6��0.5min���ѵ�ͨ������0.025mol��ת�Ƶ�����0.3mol�����ݵ�ʧ�����غ㣬Cu2++2e-=Cu�����յ�0.15molͭ����������9.6g��
���㣺���黯ѧ�빤ҵ����ϵ�������Ի�����Ӱ�죬��˹���ɶ�Ӧ�ã���ѧƽ�����۵�Ӧ�ã��绯ѧԭ����Ӧ��
�����Ѷȣ�����
3�������� ���淴ӦA��g����B��g�� C��g���������ݻ���ȵ������зֱ����A��B��1mol����һ��������700Kʱ�ﵽƽ�⣬ѹǿΪԭ����75�����ڶ���������900Kʱ�ﵽƽ�⣬�������A���������Ϊ25����ͨ�������жϸ÷�Ӧ�Ƿ��Ȼ������ȷ�Ӧ�� C��g���������ݻ���ȵ������зֱ����A��B��1mol����һ��������700Kʱ�ﵽƽ�⣬ѹǿΪԭ����75�����ڶ���������900Kʱ�ﵽƽ�⣬�������A���������Ϊ25����ͨ�������жϸ÷�Ӧ�Ƿ��Ȼ������ȷ�Ӧ��
�ο��𰸣����ȷ�Ӧ?
����������⣺
��700 Kʱ��ƽ��
A��g����B��g�� C��g�� C��g��
nʼ??? 1mol???? 1mol????? 0
��n???x???????x????????x
nƽ???? 1-x???
�����Ѷȣ�һ��
4��ѡ���� �����Ȼ�ѧ����ʽ�С�H����ȼ���ȵ��� [???? ]
A��CH4(g)+O2(g)==2H2O(l)+CO(g) ��H1
B��S(s)+3/2O2(g)==SO3 (S) ��H2
C��C6H12O6(s)+6O2(g)==6CO2(g)+6H2O(l) ��H3
D��2CO(g)+O2(g)==2CO2(g) ��H4
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ȼ�����뷴Ӧ�ȵĹ�ϵ��
A����һ����Ӧ��ȼ�շ�Ӧʱ����ȼ�շ�Ӧ�ķ�Ӧ�Ⱦ���ȼ����
B��ȼ�����Ƿ�Ӧ�ȵ�һ������
C��ȼ���Ȳ����ڷ�Ӧ��,��Ӧ������25 �桢101 kPa�²ⶨ�ģ���ȼ�շ�Ӧ���¶�Ҫ��
D����Ӧ��������֮�֣�ȼ����ȫ������ֵ
�ο��𰸣�B
���������
���������ȼ���ȱ��������ȶ���������ʱ�ų�����������ȼ�շ�Ӧ��һ�������ȶ����������Ӧ�Ȳ�һ����ȼ���ȣ�A����ȼ������һ�������µķ�Ӧ�����ڻ�ѧ��Ӧ�ķ�Ӧ�ȣ���B��ȷ��ȼ�����Ƿ�Ӧ�ȵ�һ�����ͣ����߷�Ӧ��������ͬ�ģ�C����ȼ����ȫ���Ƿ��ȷ�Ӧ��ȫ��Ϊ��ֵ��D����
���㣺��Ӧ�ȣ�ȼ����
�����Ѷȣ�һ��
|