微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g) 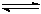 ?Si3N4(s)? + 6CO(g)
?Si3N4(s)? + 6CO(g)
(1)该反应的氧化剂是???????????????,2molN2参加反应转移电子数为???????????????;
(2)该反应的平衡常数表达式为K= ????????? ;
(3)若CO的生成速率为v(CO)=18mol・L-1・min-1,则N2的消耗速率为v(N2)=?????????
(4)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图。图中t4时引起平衡移动的条件可能是?????????????????????;图中表示平衡混合物中CO的含量最高的一段时间是???????????。

(5)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是??????????????(提示:272 = 729)
参考答案:(1)氮气 (1分) ??12NA? (1分)(2)K=[c
本题解析:
试题分析:(1)反应中N元素的化合价降低,有0价降为-3价,则氧化剂为氮气,氧化剂对应的生成物为还原产物,应为氮化硅,故答案为:氮气;氮化硅;(2)平衡常数等于气体生成物的浓度幂之积除以气体反应物的浓度幂之积,则K=[c(CO)]6/[c(N2)]2(3)反应放热,△H<0,升高温度平衡移动逆反应方向移动,平衡常数减小,速率之比等于化学计量数之比,则v(N2)=1/3×v(CO)=1/3×18mol?L-1?min?1="6" mol?L-1?min?1(4) t4时正逆反应速率都较原平衡时的速率
本题难度:困难
2、选择题 已知:C(s)+CO2(g)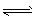 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是 [???? ]
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是 [???? ]
A.升高温度和减小压强
B.降低温度和减小压强
C.降低温度和增大压强
D.升高温度和增大压强
参考答案:A
本题解析:
本题难度:一般
3、简答题 在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物.各种生成物在平衡体系内的分压与反应温度的关系如图所示(己知气体的分压之比等于物质的量之比).
(1)420K时,发生反应的化学方程式为:______;若反应中消耗l?mol?Xe,则转移电子______mol.
(2)600~800K时,会发生反应:XeF6(g)?

XeF4(g)+F2(g),
其反应热△H______0(填“>”“=”或“<”).理由是______.
(3)900K时,容器中存在的组分有______.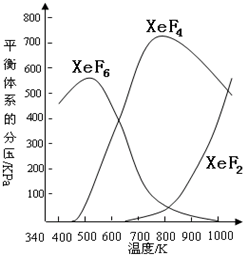
参考答案:(1)在420K时,产物只有XeF6,故其反应方程式为:Xe
本题解析:
本题难度:一般
4、选择题 已知热化学方程式:SO2(g)+ O2(g) 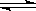 SO3(g) △H ="
SO3(g) △H ="
参考答案:
本题解析:
本题难度:一般
5、填空题 (Ⅰ)已知在448℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)?H2(g)+I2(g)的平衡常数K2为______;反应
1
2
H2(g)+1
2
I2(g)?HI(g)的平衡常数K3为_______.
(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
| t/℃ | 700 | 800 | 830 | 1000 | 1200
K
0.6
0.9
1.0
1.7
2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K=______.
(2)该反应为______反应(填“吸热”或“放热”).
(3)能判断该反应达到化学平衡状态的依据是______.
A.容器中压强不变???????????B.混合气体中C(CO)不变
C.V(H2)正=V(H2O)逆????? D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:C(CO2)?C(H2)=c(CO)?c(H2O),判断此时温度为______℃.
参考答案:(Ⅰ)448℃时,反应H2(g)+I2(g)?2HI(g)的
本题解析:
本题难度:一般
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772