微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 若某氖原子质量是a?g,12C的原子质量是b?g,NA是阿伏加德罗常数的值,下列说法正确的是
A.氖元素的相对原子质量一定是12a/b
B.该氖原子的摩尔质量是aNAg
C.Wg该氖原子的物质的量一定是mol
D.Wg该氖原子所含质子数是10W/a
参考答案:C
本题解析:分析:A、根据元素的相对原子质量含义计算;
B、依据摩尔质量概念分析计算;
C、根据物质的量的概念计算;
D、质量换算为物质的量进而计算质子数;
解答:A、氖原子的相对原子质量= =
= ,氖元素存在同位素,氖元素的相对原子质量是同位素所占体积分数的平均值,故A错误;
,氖元素存在同位素,氖元素的相对原子质量是同位素所占体积分数的平均值,故A错误;
B、氖原子的摩尔质量是1mol原子的质量即aNAg?mol-1,故B错误;
C、Wg该氖原子的物质的量= =
= mol,故C正确;
mol,故C正确;
D、Wg该氖原子所含质子数=1mol氖原子所含质子数×物质的量=2× ,故D错误;
,故D错误;
故选C
点评:本题考查了原子相对原子质量、元素相对原子质量、摩尔质量、物质的量等概念的理解与应用.
本题难度:困难
2、选择题 20℃时有a?g硫酸铜溶液V?mL,将溶液蒸发掉b?g水后恢复到20℃,恰好全部生成硫酸铜晶体(CuSO4?5H2O),则下列关系式错误的是
A.原硫酸铜溶液的密度为
B.生成硫酸铜晶体的物质的量为
C.原硫酸铜溶液的物质的量浓度为
D.原硫酸铜溶液的质量分数ω(CuSO4)=%
参考答案:C
本题解析:分析:A、根据密度定义ρ=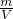 计算.
计算.
B、硫酸铜晶体的质量为(a-b)g,根据n= 计算生成硫酸铜晶体的物质的量.
计算生成硫酸铜晶体的物质的量.
C、硫酸铜晶体的质量为(a-b)g,所以硫酸铜的物质的量为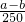 mol,根据c=
mol,根据c=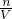 计算硫酸铜溶液的物质的量浓度.
计算硫酸铜溶液的物质的量浓度.
D、硫酸铜晶体的质量为(a-b)g,所以硫酸铜的物质的量为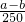 mol,据此计算硫酸铜的质量,溶液质量为ag,根据质量分数定义计算.
mol,据此计算硫酸铜的质量,溶液质量为ag,根据质量分数定义计算.
解答:A、Vml硫酸铜溶液质量ag,所以溶液的密度为ρ=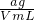 =ag/mL,故A正确;
=ag/mL,故A正确;
B、硫酸铜晶体的 91eXaM.org质量为(a-b)g,生成硫酸铜晶体的物质的量为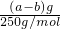 =
=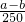 mol,故B正确;
mol,故B正确;
C、硫酸铜晶体的质量为(a-b)g,生成硫酸铜晶体的物质的量为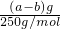 =
=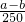 mol,所以原硫酸铜溶液的
mol,所以原硫酸铜溶液的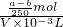 =
=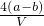 mol/L,故C错误;
mol/L,故C错误;
D、硫酸铜晶体的质量为(a-b)g,所以硫酸铜的物质的量为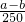 mol,故原硫酸铜溶液的质量分数ω(CuSO4)=
mol,故原硫酸铜溶液的质量分数ω(CuSO4)=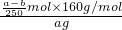 ×100%=
×100%=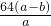 %,故D正确.
%,故D正确.
故选:C.
点评:考查物质的量浓度、溶质质量分数、溶液密度等计算,难度中等,注意公式运用,判断硫酸铜晶体的质量是关键.
本题难度:一般
3、选择题 下列说法正确的是
A.NaOH的摩尔质量为40?g
B.1?mol?02 的质量与它的相对分子质量相等
C.1?mol?OH-的质量为17 g?mol-1??
D.氖气的摩尔质量(单位g?mol-1)在数值上等于它的相对原子质量
参考答案:D
本题解析:分析:A、摩尔质量是单位物质的量的 物质的质量;单位是g/mol;
B、1 mol 02 的质量与它的相对分子质量数值上相等;
C、质量单位是g;
D、氖气是单原子分子,它的摩尔质量在数值上等于它的相对原子质量.
解答:A、NaOH的摩尔质量为40 g/mol,故A错误;
B、1 mol 02 的质量数值上与它的相对分子质量相等,故B错误;
C、1 mol OH-的质量为17 g,故C错误;
D、氖气是单原子分子,氖气的摩尔质量(单位g?mol-1)在数值上等于它的相对原子质量,故D正确;
故选D.
点评:本题考查了摩尔质量的概念和计算应用,理解概念的实质和数值确定,单位判断是解题关键,题目较简单.
本题难度:一般
4、选择题 下列过程不属于化学变化的是
A.煤的干馏
B.石油的分馏
C.石油的裂解
D.蔗糖的水解
参考答案:B
本题解析:分析:化学变化是指在原子核不变的情况下,有新物质生成的变化.物理变化是指没有新物质生成的变化.化学变化和物理变化的本质区别在于是否有新物质生成.
解答:A.煤的干馏过程中有新物质生成,属于化学变化,故A错误;
B.石油的分馏变化过程中没有新物质生成,属于物理变化,故B正确;
C.石油的裂解是一种使烃类分子分裂为几个较小分子的反应过程,有新物质生成,属于化学变化,故C错误;
D.蔗糖水解生成葡萄糖和果糖,有新物质生成,属于化学变化,故D错误.
故选B.
点评:本题考查物理变化与化学变化的区别与联系,难度不大,解答时要分析变化过程中是否有新物质生成,这里的新物质是指和变化前的物质是不同种的物质,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.
本题难度:困难
5、选择题 用NA表示阿伏加德罗常数,下列说法正确的是
A.17g羟基中所含电子数为10NA
B.标准状况下,2.24?LCHCl3含有的分子数为0.1NA
C.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,Na失去的电子数为NA
D.100g质量分数为98%的浓硫酸中含氧原子数为4NA
参考答案:C
本题解析:分析:A、依据n=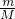 计算物质的量,结合羟基结构计算羟基电子数;
计算物质的量,结合羟基结构计算羟基电子数;
B、标准状况下,CHCl3不是气体;
C、钠全部反应失去电子依据反应的钠计算;
D、依据溶质质量=溶液质量×溶质质量分数,结合溶质中氧原子数计算;
解答:A、17g羟基物质的量为1mol,所含电子数为9NA,故A错误;
B、标准状况下,CHCl3不是气体,2.24 LCHCl3含物质的量不是0.1mol,故B错误;
C、1molNa与足量O2反应,钠全部反应失去电子依据反应的钠计算,生成Na2O和Na2O2的混合物,Na失去的电子数为NA,故C正确;
D、100 g质量分数为98%的浓硫酸中溶质质量为98g,溶质硫酸物质的量为1mol,溶液中含氧原子数大于4NA,故D错误
故选C.
点评:本题考查了阿伏伽德罗常数的应用,主要是质量换算物质的量计算微粒数,气体摩尔体积的条件应用,物质构成分析,题目难度中等.
本题难度:一般