微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组物质中分子数相同的是
A.2LCO和2LCO2
B.9gH2O和标准状况下11.2LCO2
C.标准状况下1molO2和22.4LH2O
D.0.2molH2和4.48LHCl气
参考答案:B
本题解析:分析:在标准状况下,气体的Vm=22.4L/mol,根据气体含有的分子数N=nNA= NA=
NA= NA来计算.
NA来计算.
解答:A、相同条件下,相同体积的任何气体具有相同的分子数,故A错误;
B、9gH2O的分子数N= NA=
NA= NA=0.5NA,,标准状况下11.2LCO2的分子数N=
NA=0.5NA,,标准状况下11.2LCO2的分子数N= NA=
NA=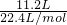 NA=0.5NA,即9gH2O和标准状况下11.2LCO2中分子数相同,故B正确;
NA=0.5NA,即9gH2O和标准状况下11.2LCO2中分子数相同,故B正确;
C、标准状况下1molO2的分子数为NA,22.4LH2O的分子数不是NA,因为标况下的水不是气态,故C错误;
D、0.2molH2的分子数为0.2NA,4.48LHCl气体在标况下的分子数才是0.2NA,题干没指名状态,所以4.48LHCl气体的分子数不一定是0.2NA,故D错误.
故选B.
点评:本题考查学生摩尔体积的相关计算,可以根据所学知识来回答,难度不大.
本题难度:困难
2、选择题 用NA表示阿伏加德罗常数,下列说法正确的是
A.在0℃,压强为101×105Pa时,22.4L?Cl2与HCl的混合气体中含有的氯原子总数为3NA
B.0.5molI-被氧化时失去的电子数为0.5NA
C.0.1L3?mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023
D.常温常压下,48gO3含有氧原子数为3NA
参考答案:D
本题解析:分析:A、在0℃,压强为101×105Pa时是标准状况,体积换算物质的量结合分子式计算;
B、依据碘离子可以被氧化为碘单质或碘酸根;
C、铵根离子水解;
D、质量换算物质的量结合分子式计算氧原子数;
解答:A、标准状况下,22.4L Cl2与HCl的混合气体物质的量为1mol,含氯原子在1mol-2mol间,故A错误;
B、碘离子可以被氧化为碘单质或碘酸根,所以氧化产物不定,故B错误;
C、铵根离子水解,0.1L3 mol?L-1的NH4NO3溶液中含有的NH4+数目小于0.3×6.02×1023;故C错误;
D、48gO3物质的量为1mol,含有氧原子数为3NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,氧化还原反应的产物判断,盐类水解的应用.
本题难度:一般
3、选择题 下列各组物质中,所含分子数目相同的是
A.10gH2和10gO2
B.9gH2O和0.5molBr2
C.224mLH2(标准状况)和0.1molN2
D.5.6LN2和11gCO2
参考答案:B
本题解析:分析:A.根据n=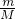 计算氢气、氧气的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
计算氢气、氧气的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
B.根据n=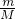 计算水的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
计算水的物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
C.根据n=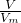 计算氢气物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
计算氢气物质的量,根据N=nNA可知,物质的量越大,含有分子数目越大;
D.未指明氮气所处的状态,气体摩尔体积不一定是22.4L/mol.
解答:A.10gH2的物质的量=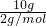 =5mol,10gO2的物质的量=
=5mol,10gO2的物质的量=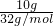 =
=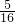 mol,二者物质的量不相等,含有的分子数目不相等,故A错误;
mol,二者物质的量不相等,含有的分子数目不相等,故A错误;
B.9gH2O的物质的量=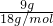 =0.5mol,与0.5molBr2的物质的量相等,含有的分子数目相等,故B正确;
=0.5mol,与0.5molBr2的物质的量相等,含有的分子数目相等,故B正确;
C.224mLH2(标准状况)的物质的量=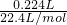 =0.01mol,与0.1molN2的物质的量不相等,二者含有的分子数目不相等,故C错误;
=0.01mol,与0.1molN2的物质的量不相等,二者含有的分子数目不相等,故C错误;
D.未指明氮气所处的状态,气体摩尔体积不一定是22.4L/mol,物质的量不一定是0.5mol,二者物质的量不一定相等,根据N=nNA可知,二者含有分子数目不一定相等,故D错误;
故选B.
点评:本题考查常用化学计量的有关计算,难度不大,注意对公式的理解与灵活运用,注意气体摩尔体积的使用条件与对象.
本题难度:困难
4、选择题 下列有关溶液的说法中,正确的是
A.含H+的溶液显酸性,含OH-的溶液显碱性
B.用丁达尔现象实验可区分葡萄糖溶液和氢氧化铁胶体
C.某饱和溶液变成不饱和溶液,溶质的质量分数一定减小
D.标准状况下,2.24?L?NH3溶于水制得1L氨水,则c?(NH3?H2O)=0.1mol?L-1
参考答案:B
本题解析:分析:A.溶液的酸碱性取决于溶液中氢离子浓度与氢氧根离子浓度的相对大小;
B.胶体有丁达尔效应;
C.在不指明温度的情况下饱和与不饱和溶液溶质质量分数无法比较;
D.NH3?H2O是弱电解质.
解答:A.判断溶液的酸碱性应根据溶液中氢离子浓度与氢氧根离子浓度的相对大小判断,故A错误;
B.溶液无丁达尔效应,胶体有丁达尔效应,可用丁达尔效应可以区别溶液与胶体,故B正确;
C.在不指明温度的情况下饱和与不饱和溶液溶质质量分数无法比较大小,相同温度饱和溶液一定比不饱和溶液质量分数要大,故C错误;
D.NH3?H2O是弱电解质,能发生部分电离,浓度小于0.1mol?L-1,故D错误.
故选B.
点评:本题考查酸碱的定义、胶体的性质、饱和溶液、弱电解质的电离等,难度不大,注意溶液的酸碱性取决于溶液中氢离子浓度与氢氧根离子浓度的相对大小.
本题难度:一般
5、选择题 H2O2的摩尔质量为
A.18g
B.34g
C.18g/mol
D.34g/mol
参考答案:D
本题解析:分析:根据摩尔质量在以g/mol为单位时,在数值上等于其相对分子质量.
解答:因H2O2的相对分子质量为34,所以H2O2的摩尔质量为34g/mol,故选:D.
点评:本题主要考查的是摩尔质量及其单位,根据与相对分子质量的关系即可判断,难度不大.
本题难度:一般