��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �п��Ľ���Na��¶�ڿ����У���仯�������£�

��1����Ӧ��ķ�Ӧ�����������仯�Ĺ�ϵ���£�
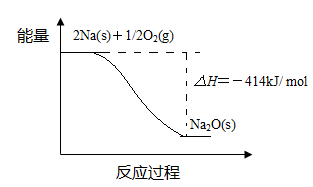
�� ��Ӧ�� ���� ����Ӧ������ȡ������ȡ������ж���������������
�� 1 mol Na(s)ȫ��������Na2O(s)���Ȼ�ѧ����ʽ����������
��2����Ӧ����Na2O��ˮ�ķ�Ӧ�������ĵ���ʽ��?????��
��3����ɫ��ĩΪNa2CO3����������ˮ����Ϊ0.1 mol/L Na2CO3��Һ������˵����ȷ����?????������ĸ����
A�������¶ȣ���Һ��pH����
B��c(OH��)��c (H��)��c (HCO3��)��2 c (H2CO3)
C����������NaOH���壬c (CO32�D)��c (Na��)������
D��c (Na��) > c (CO32�D) > c (HCO3�D) > c(OH�D) > c (H��)
��4�� �Ƶ�ص��о�������һ���̶��Ͽɻ��������Դ��ȱ�����ĵ�ط�չ�������⡣
�� �Ʊ�﮻��ã���ԭ�ӽṹ����ԭ��_______��
��ZEBRA �����һ���Ƶ�أ��ܷ�ӦΪNiCl2 + 2Na  ?Ni + 2NaCl����������Ӧʽ��_____��
?Ni + 2NaCl����������Ӧʽ��_____��
�ο��𰸣���1���ٷ���????��Ӧ������������������������
��
���������
�����������1�������ڷ�Ӧ�������������������������ߣ����Է����ķ�Ӧ���Ƿ��ȷ�Ӧ���� ����Ŀ�ṩ��������ϵ�ɵø÷�Ӧ���Ȼ�ѧ����ʽΪ��Na(s)��1/4O2(g)��1/2Na2O(s) ��H����207 kJ/ mol����2����Ӧ����Na2O��ˮ�ķ�Ӧ��Na2O��ˮ��Ӧ����NaOH����Ӧ�ķ���ʽΪNa2O��H2O =2NaOH��NaOH�ĵ���ʽΪ��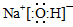 �����Ѷȣ�һ��
�����Ѷȣ�һ��
2�������� ��8�֣���NaOH��Һ��ͨ��CO2�����ַ�Ӧ���ڵ�ѹ�͵����£�С�ĵؽ���Һ���ɣ��õ���ɫ�Ĺ���M��ͨ��CO2�����V(CO2)����״������M������W�Ĺ�ϵ����ͼ��

��1��A��ʱ��M�Ļ�ѧʽΪ_____________��
��2��C��ʱ��ͨ��CO2��������Ϊ____________��
��3��B��ʱ��M����ɳɷֵĻ�ѧʽ�������ʵ���Ϊ?????????????????????????????��
�ο��𰸣�(8��)
��1��Na2CO3????????��2�֣�?
�����������
�����Ѷȣ�һ��
3�������� ��4�֣���Na2O��Na2O2��ɵĹ�����������һ������ˮ�У���ַ�Ӧ���ռ�����״���µ�����1.12L��ͬʱ�õ�0.6mol NaOH������㣺
��1��ԭ����������Na2O��Na2O2��������
��2��ǡ���к�������Һ�������2.0 mol/L HCl��Һ�������
�ο��𰸣���1��12.4 g �� 7.8 g ����1�֣�����2�� 30
�����������
�����Ѷȣ���
4������� ��6�֣�����A����AԪ����ɵĵ��ʣ������ھƾ��ƻ��������գ� ����Ϊ��ɫ��B��C��D�Ǻ���AԪ�ص����ֲ�ͬ�����A��B��C��D����ͼ��ϵ����ת����
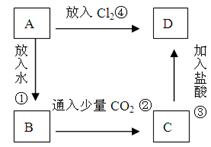
��д����ѧʽ��B??????????????????C???????????
��д���٢ڷ�Ӧ�Ļ�ѧ����ʽ��
��????????????????????????????????????
��???????????????????????????????????
�ο��𰸣���1��B??? NaOH��C??? Na2CO3?��
���������
����������ɻ���Ϊ��ɫ��֪A�ǽ����Ƶ��ʣ�A��Na����ˮ��Ӧ����B��NaOH����������B��NaOH��������CO2��Ӧ����C��Na2CO3����C��Na2CO3�������ᷴӦ����D��NaCl����
��������Ϥ����Ԫ�ؼ��仯�����ת����Ӧ
�����Ѷȣ�һ��
5��ѡ���� ��Na2O2Ͷ��FeCl3��Һ��, �ɹ۲쵽�������ǣ�??��
A�����ɰ�ɫ����
B�����ɺ��ɫ����
C����ը
D���ޱ仯
�ο��𰸣�B
���������
���������Na2O2Ͷ��FeCl3��Һ�к�Na2O2������ˮ��Ӧ��2Na2O2+2H2O=4NaOH+O2����NaOH����FeCl3��Ӧ���ɺ��ɫ������3NaOH+FeCl3=Fe(OH)3(��������+3NaCl��2O2������Һ�ķ�Ӧ
������ע��Na2O2Ͷ������Һ�У�Na2O2������ˮ��Ӧ�����ɵ�NaOH��������Һ��Ӧ��
�����Ѷȣ���