微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学反应中旧键断裂需要_____能量 [???? ]
A.?吸收??????
B.?放出??????
C.?不吸收也不放出????
D.?不一定
参考答案:A
本题解析:
本题难度:简单
2、填空题 已知:
2H2(气)+O2(气)=2H2O(气)+Q1???2H2(气)+O2(气)=2H2O(液)+Q2
2CO(气)+O2(气)=2CO2(气)+Q3
(1)关于Q1和Q2的关系正确的是______。
A.Q1>Q2
B.Q1<Q2
C.Q1=Q2
D.无法比较
你选择该答案的理由是______。
(2)CO和H2分别燃烧生成CO2和H2O(气),欲得到相同的热量,所需CO和H2的体积比是______。
参考答案:(1)B.液态水变成气态水需吸收热量或气态水变成液态水能放出
本题解析:(1)由于状态不同,反应热不同,所以写热化学方程式时,一定要注明各物质的聚集状态。否则判为错误(注:偶有通常状况为气体的物质不写其状态,即默认为气体);(2)设CO为nCOmol,H2为nH2mol,因气体的体积比等于物质的量之比(T,P一定时)。由题可知:
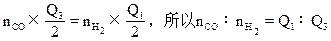
本题难度:一般
3、实验题 (10分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol・ L-1盐酸、0.55mol・L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”)。
(3)他们记录的实验数据如下:已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18kJ・℃-1・ kg-1,各物质的密度均为1g・cm-3。①计算完成下表。(保留小数点后一位)

②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,测定所得的中和热的数值将 (填“变大”或“变小”或“无影响”)。
参考答案:(10分)(1)量筒、温度计(共2分)
(2)否;金属
本题解析:
试题分析:(1)中和热的测定实验中,需要量筒量取液体,需要温度计测量溶液的温度,所以还需要量筒、温度计;
(2)不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,因为金属易导热,热量散失导致误差大;
(3)①两次实验中溶液的体积功100mL,则溶液的总质量是100g,温度升高的平均值是(23.3-20+23.5-20) ℃/2=3.4℃,根据Q=Cm(t2 -t1)计算该反应中放出的热量Q="4.18" kJ・℃-1・ kg-1×0.1kg×3.4℃=1.4212kJ,则中和热是生成1mol水放出的热量,HCl不足,按HCl的量进行计算,所以△H=-1.4212kJ/(0.5mol/L×0.05L)=-56.8kJ/mol;
②所以氢氧化钠与HCl溶液反应的热化学方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8kJ/mol;
(4)KOH与NaOH都是一元强碱,所以对结果无影响;若用醋酸代替HCl做实验,因为醋酸是弱酸,电离需要吸收热量,则放出的热量少,测定所得的中和热的数值将变小。
考点:考查中和热的测定实验,仪器的选择,中和热的计算与判断,热化学方程式的书写
本题难度:一般
4、选择题 以共价单键相连的非金属单质中,1个原子与相邻原子成键的数目为(8-N)个,N为该非金属元素的族序数,这一现象被化学家称为8-N规则.某非金属单质的结构如图所示,构成该单质的元素位于( )
A.第ⅢA族
B.第ⅣA族
C.第ⅤA族
D.第ⅥA族
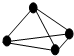
参考答案:观察分子结构图,不难发现该分子中,一个原子与另外3个原子成键
本题解析:
本题难度:一般
5、选择题 下列说法正确的是
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.某反应ΔH=-122KJ・mol-1,ΔS=231J・mol-1・k -1,此反应任何温度下都不能自发进行
C.活化分子之间发生的碰撞不一定为有效碰撞
D.对有气体参加的化学反应,减小体积增大体系压强,可使单位体积内活化分子数增加,因而反应速率增大
参考答案:CD
本题解析:
试题分析:根据△G=△H-T・△S可知,只有△G小于0时,反应才是自发的,A不正确;B中反应任何温度下都能自发进行,B不正确;选项CD正确,答案选CD。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力和抽象思维能力。
本题难度:简单