��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
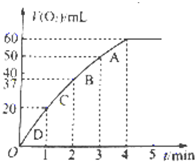
1������� I��ʵ����0.01mol/L��KMnO4��������Һ��0.1mol/L��H2C2O4��Һ�������Ϻ�Ӧ���ʦ�[mol/��L?s��]�뷴Ӧʱ��t��s���Ĺ�ϵ��ͼ��ʾ���ش��������⣺
��1���÷�Ӧ�Ļ�ѧ����ʽ��______
��2��0��t2ʱ����ڷ�Ӧ���������ԭ���ǣ�______��
��3��t2��tʱ����ڷ�Ӧ���ʼ�С��ԭ���ǣ�______��
��4��ͼ����Ӱ���֡��������ʾt1��t3ʱ����______��
A��Mn2+���ʵ���Ũ�ȵ�����????????????B��Mn2+���ʵ���������
C��SO42-���ʵ���Ũ��???????????????????D��MnO4-���ʵ���Ũ�ȵļ�С
��Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����ij��ѧ�о�С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�飮��ش�������⣺

?
��1�����Է�������ͼ�ɹ۲�______�����ԱȽϵó����ۣ���ͬѧ�����FeCl3��ΪFe2��SO4��3��Ϊ��������������______��
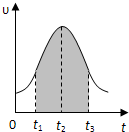
��2��������������ͼ����ʾ��ʵ��ʱ��������40mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԣ�ͼ������A������Ϊ______��ʵ������Ҫ������������______
��3������0.01mol?MnO2��ĩ��60mL?H2O2��Һ�У��ڱ�״���·ų����������ʱ��Ĺ�ϵ��ͼ��ʾ����ų�����������ΪV?mL��
�ٷų�
V
3
mL����ʱ����ʱ��Ϊ______min��
�ڸ�H2O2��Һ��Ũ��Ϊ______
��A��B��C��D���㷴Ӧ���ʿ�����˳��Ϊ______��______��______��______��
�ο��𰸣�I��1���÷�Ӧ�ķ�Ӧ����KMnO4�� H2C2O4���������
���������
�����Ѷȣ�һ��
2������� ��14�֣��״�����Ϊ21���͵�����ȼ�ϣ���ҵ��ͨ�����з�Ӧ�ٺ͢ڣ���CH4��H2OΪԭ�����Ʊ��״�����CH4��g����H2O ��g�� CO��g����3H2��g��??��H1???��CO��g����2H2��g�� CO��g����3H2��g��??��H1???��CO��g����2H2��g�� CH3OH��g����H2?��0��2mol CH4��0��3mol H2O��g��ͨ���ݻ�Ϊ10L���ܱ������У���һ�������·�����Ӧ�٣��ﵽƽ��ʱ��CH4��ת�������¶ȣ�ѹǿ�Ĺ�ϵ��ͼ��ʾ�� CH3OH��g����H2?��0��2mol CH4��0��3mol H2O��g��ͨ���ݻ�Ϊ10L���ܱ������У���һ�������·�����Ӧ�٣��ﵽƽ��ʱ��CH4��ת�������¶ȣ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
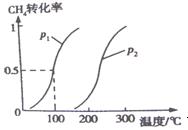
��1���¶Ȳ��䣬��С���������ѹǿ���ٵķ�Ӧ����?????????????�����������С���������䡱����ƽ����???????????�����ƶ���
��2����Ӧ�ٵġ�H1???????0���������������������������ƽ�ⳣ������ ʽΪK=???????????????��100�棬ѹǿΪp1ʱƽ�ⳣ����ֵ��????????????????�� ʽΪK=???????????????��100�棬ѹǿΪp1ʱƽ�ⳣ����ֵ��????????????????��
��3����ѹǿΪ0��1Mpa�����£���a mol CO��3a molH2�Ļ�������ڴ��������½��з�Ӧ�ڡ�Ϊ��Ѱ�Һϳɼ״����¶Ⱥ�ѹǿ������������ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С������¿ո�������ʣ���ʵ���������ݡ�
ʵ����
| T��
| n��CO��/n��H2��
| p ��Mpa��
| I
| 150
| 1/3
| 0��1
| ��
| ?
| ?
| 5
| ��
| 350
| ?
| 5
��4�������꿪���ļ״�ȼ�ϵ���Dz��ò��缫������е����ӽ���Ĥֻ�������Ӻ�ˮ����ͨ�����乤��ԭ��ʾ��ͼ���£�
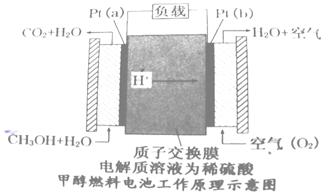
��ش�
��Pt��a���缫�ĵ缫��ӦʽΪ???????????????????????????????????????????
������õ�ع���ʱ��·��ͨ��2mol���������ĵ�CH3OH��??????????mol��
�ο��𰸣���1������1�֣�??�淴Ӧ��������1�֣�
��2��
�����������
�����Ѷȣ�һ��
3��ѡ���� ��0.6 mol X�����0.4 mol Y��������2 L�����У�ʹ���Ƿ������·�Ӧ��3X(g)��Y(g)===nZ(g)��2W(g)����5 minʱ�Ѿ�����0.2 mol W������֪��Z��Ũ�ȱ仯��ʾƽ����Ӧ����Ϊ0.01 mol��L��1��min��1����������Ӧ��Z����Ļ�ѧ������n��ֵ��(����)
A��4
B��3
C��2
D��1
�ο��𰸣�D
���������
���������????????3X(g)??��?? Y(g)??===??? nZ(g)?��?? 2W(g)
��ʼ?????? 0.6mol?????? 0.4mol?????????0????????? 0
�仯??????0.3mol?????? 0.1mol???????? 0.1nmol??? 0.2mol
5minʣ��???? 0.3mol?????? 0.3mol???????? 0.1nmol???? 0.2mol
�������ʹ�ʽ��֪v(Z)= �����Ѷȣ��� �����Ѷȣ���
4������� ��12�֣���2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)+O2(g)�P2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s)
| 0
| 1
| 2
| 3
| 4
| 5
| n(NO)/(mol)
| 0.020
| 0.010
| 0.008
| 0.007
| 0.007
| 0.007
?(1)д���÷�Ӧ��ƽ�ⳣ������ʽ��K=???????????????????????��
��֪��K��300�棩��K(350��)���÷�Ӧ��_????????????????��
(2)��ͼ�б�ʾNO2�ı仯��������?????????????????��
��O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ������v=?????????????��
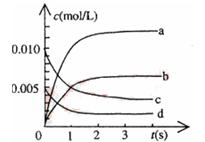
(3)��˵���÷�Ӧ�Ѵﵽƽ��״̬����???????????????????��
a��v(NO2)=2v(O2)???????????? b��������ѹǿ���ֲ���
c��v��?(NO)=2v�� (O2)?????? d���������ܶȱ��ֲ���[
(4)Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����??????????????��
a����ʱ�����NO2����?????????? b���ʵ������¶�
c������O2��Ũ��??????????????? d��ѡ���Ч����
�ο��𰸣�
 ����������� �����������
�����Ѷȣ�һ��
5��ѡ���� ������ɱ�������з�����ӦN2 + 3H2  ?NH3������ѹǿʹ���������Сʱ����ѧ��Ӧ���ʼӿ죬����Ҫԭ���ǣ�????�� ?NH3������ѹǿʹ���������Сʱ����ѧ��Ӧ���ʼӿ죬����Ҫԭ���ǣ�????��
A�������˶����ʼӿ죬ʹ��Ӧ����Ӽ����ײ��������
B����Ӧ����ӵ��������ӣ�����Ӱٷ���������Ч��ײ��������
C�����Ӽ�����С��ʹ���еĻ���Ӽ����ײ����Ϊ��Ч��ײ
D������Ӱٷ���δ�䣬����λ����ڻ���������ӣ���Ч��ײ��������
�ο��𰸣�D
���������������ѹǿʹ���������Сʱ����ѧ��Ӧ���ʼӿ죬��λ����ڻ���������ӣ���Ч��ײ�������࣬������Ӱٷ������䡣
�����Ѷȣ���
|
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772