微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在10 mL 0.1 mol/L NaOH溶液中加入等体积、等浓度的CH3COOH溶液,反应后溶液中各粒子的浓度关系错误的是
A.C(Na+)>C(CH3COO-)>C(H+)>C(OH-)
B.C(Na+)>C(CH3COO-)>C(OH-)>C(H+)
C.C(Na+)= C(CH3COO-)+C(CH3COOH)
D.C(Na+)+ C(H+)= C(CH3COO-)+C(OH-)
参考答案:A
本题解析:
试题分析:10 mL 0.1 mol/L NaOH溶液中加入等体积、等浓度的CH3COOH溶液,酸碱恰好反应生成CH3COONa ,CH3COONa属于强碱弱酸盐,CH3COO-会水解导致溶液显碱性,CH3COO-浓度减小,所以反应后溶液中各粒子的浓度关系为C(Na+)>C(CH3COO-)>C(OH-)>C(H+),A项错误;B项正确;C项符合物料守恒,正确;D项符合电荷守恒,正确;选A。
考点:考查溶液中离子浓度的大小比较。
本题难度:一般
2、选择题 下列化学方程式中,属于水解反应的是
A.H2O+H2O H3O++OH-
H3O++OH-
B.HCO3-+OH- H2O+CO32-
H2O+CO32-
C.CO2+H2O H2CO3
H2CO3
D.CO32-+H2O HCO3-+OH-
HCO3-+OH-
参考答案:D
本题解析:
正确答案:D
A、水电离方程式;B、化学反应的离子方程式;C、化学反应方程式;D、水解反应离子方程式。
本题难度:一般
3、选择题 在0.1 mol/L的Na2CO3溶液中,下列关系正确的是( )
A.c(Na+)=2c(CO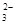 )
)
B.c(OH-)=2c(H+)
C.c(HCO )>c(H2CO3)
)>c(H2CO3)
D.c(Na+)<c(CO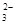 )+c(HCO
)+c(HCO )
)
参考答案:C
本题解析:
试题分析:A.根据物料守恒可得c(Na+)=2c(CO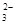 ) +2c(HCO
) +2c(HCO ) +2c(H2CO3),错误;B.由于溶液显碱性,所以根据质子守恒可得:c(OH-)=c(H+)+ c(HCO3-) +2c(H2CO3),错误;C.因为酸的电离程度:H2CO3> HCO3。酸越弱,其离子水解程度就越大,微粒的浓度就越小,所以c(HCO
) +2c(H2CO3),错误;B.由于溶液显碱性,所以根据质子守恒可得:c(OH-)=c(H+)+ c(HCO3-) +2c(H2CO3),错误;C.因为酸的电离程度:H2CO3> HCO3。酸越弱,其离子水解程度就越大,微粒的浓度就越小,所以c(HCO )>c(H2CO3)。正确;D.根据物料守恒可得:c(Na+)=2c(CO
)>c(H2CO3)。正确;D.根据物料守恒可得:c(Na+)=2c(CO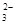 )+2c(HCO
)+2c(HCO )+2c(H2CO3),所以c(Na+)>c(CO
)+2c(H2CO3),所以c(Na+)>c(CO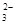 )+c(HCO
)+c(HCO ),错误。
),错误。
考点:考查溶液中离子浓度的大小比较的知识。
本题难度:一般
4、选择题 下列有关问题与盐的水解有关的是 [???? ]
①NH4Cl与ZnCl2溶液可用作焊接金属时的除锈剂
②NaHCO3与Al2 (SO4)3两种溶液可作泡沫灭火剂
③某CH3COOH和CH3COONa的混合溶液中c(Na+) =c(CH3COO-)
④实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞
A.①②③
B.②③④
C.①④
D.①②③④
参考答案:D
本题解析:
本题难度:一般
5、填空题 (8分)
I.已知在25℃时,HF、HCN和H2CO3的的电离平衡常数如表所示:
(1)写出碳酸的第一级电离平衡常数表达式:K1= 。
(2)①往Na2CO3溶液中加入足量HF溶液,发生反应的离子方程式:
②往NaCN溶液中通入少量CO2,发生反应的离子方程式:
II. 用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2・6H2O时,能得到无水MgCl2,其原因是 。
参考答案:)I. (1) 本题解析:
本题解析:
试题分析:(1)碳酸是二元弱酸,分别电离,碳酸的第一级电离平衡常数表达式: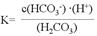 ;(2)①由于酸性HF>H2CO3,所以往Na2CO3溶液中加入足量HF溶液,发生反应的离子方程式2HF+CO32-=2F-+H2O+CO2↑;②由于酸性:H2CO3> HCN> HCO3- ,往NaCN溶液中通入少量CO2,发生反应的离子方程式是CN-+H2O+CO2= HCN+HCO3-;II. 用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2・6H2O时,能得到无水MgCl2,其原因是在干燥的HCl气流中,抑制了MgCl2的水解,且带走了MgCl2・6H2O受热产生的水蒸气,从而得到无水MgCl2。
;(2)①由于酸性HF>H2CO3,所以往Na2CO3溶液中加入足量HF溶液,发生反应的离子方程式2HF+CO32-=2F-+H2O+CO2↑;②由于酸性:H2CO3> HCN> HCO3- ,往NaCN溶液中通入少量CO2,发生反应的离子方程式是CN-+H2O+CO2= HCN+HCO3-;II. 用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2・6H2O时,能得到无水MgCl2,其原因是在干燥的HCl气流中,抑制了MgCl2的水解,且带走了MgCl2・6H2O受热产生的水蒸气,从而得到无水MgCl2。
考点:考查弱酸的电离平衡常数的应用、离子方程式的书写及盐的水解对物质制取条件的影响的知识。
本题难度:一般