微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g)?2SO3(g),△H<0的正、逆反应速率的影响如图所示:

(1)加催化剂对反应速率影响的图象是______(填序号,下同),平衡______移动.
(2)升高温度对反应速率影响的图象是______,平衡向______方向移动.
(3)增大反应容器体积对反应速率影响的图象是______,平衡向______方向移动.
(4)增大O2的浓度对反应速率影响的图象是______,平衡向______方向移动.
参考答案:(1)催化剂只影响反应速率,不影响化学平衡,所以加入催化剂后
本题解析:
本题难度:一般
2、选择题 设C+CO2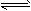 2CO-Q1(吸热反应)反应速率为u1,N2+3H2
2CO-Q1(吸热反应)反应速率为u1,N2+3H2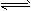 2NH3+Q2(放热反应)反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为 [???? ]
2NH3+Q2(放热反应)反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为 [???? ]
A.同时增大
B.同时减小
C.增大,减小
D.减小,增大
参考答案:A
本题解析:
本题难度:简单
3、选择题 将等质量的a、b两份锌粉装入试管中,分别加入过量的稀硫酸,同时向装a的试管中加入少量CuSO4溶液。右图表示产生氢气的体积V与时间t的关系,其中正确的是(?)
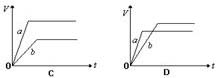
参考答案:D
本题解析:
试题分析:向装a的试管中加入少量CuSO4溶液,则锌和硫酸铜发生置换反应,生成铜,则可以构成原电池,锌是负极,加快反应速率。但由于消耗了部分锌,则生成的氢气减少,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。试题设计新颖,综合性强,侧重对学生解题能力和技巧的培养和训练,有利于培养学生的逻辑推理能力和发散思维能力,提高学生的应试能力和学习效率。该题的关键是明确原电池原理,并能结合题意灵活运用即可。
本题难度:简单
4、简答题 (15分)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H2C2O4 + 3H2SO4= K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
实验编号
| 室温下,试管中所加试剂及其用量 / mL
| 室温下溶液颜色褪至无色所需时间 / min
|
0.6 mol/L
H2C2O4溶液
| H2O
| 3 mol/L
稀硫酸
| 0.05mol/L KMnO4溶液
|
1
| 3.0
| 2.0
| 2.0
| 3.0
| 1.5
|
2
| 2.0
| 3.0
| 2.0
| 3.0
| 2.7
|
3
| 1.0
| 4.0
| 2.0
| 3.0
| 3.9
请回答:
(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)= 。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验编号
| 室温下,试管中所加试剂及其用量 / mL
| 再向试管中加入少量固体
| 室温下溶液颜色褪至无色所需时间 / min
| 0.6 mol/L
H2C2O4溶液
| H2O
| 3 mol/L
稀硫酸
| 0.05 mol/L KMnO4溶液
| 4
| 3.0
| 2.0
| 2.0
| 3.0
|
| t
③若该小组同学提出的假设成立,应观察到的现象是 。
(4)工业上可用电解K2MnO4浓溶液的方法制取KMnO4,则电解时,阳极发生的电极反应为 ;总方程式为 。
参考答案:(1)其他条件相同时,增大H2C2O4浓度(或反应物浓度),
本题解析:
试题分析:(1)根据表中数据可知,其他条件相同时,增大H2C2O4浓度(反应物浓度),反应速率增大。
(2)反应中消耗高锰酸钾的浓度是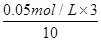 =0.015mol/L,所以υ(KMnO4)=0.015mol/L÷1.5min=1.0×10-2 mol / (L・min)。 =0.015mol/L,所以υ(KMnO4)=0.015mol/L÷1.5min=1.0×10-2 mol / (L・min)。
(3)①由图2可知反应开始后速率增大的比较快,说明生成物中的MnSO4(或Mn2+)为该反应的催化剂.
②要验证假设作对比实验与与实验1比较,其它条件相同时加入MnSO4即可。
③如果假设成立,则加入硫酸锰以后若反应加快,溶液褪色的时间小于1.5min,说明Mn2+是催化剂.
(4)K2MnO4制取KMnO4,反应过程中Mn元素的化合价从+6价升高到+7价,因此锰酸钾在阳极放电,电极反应式为MnO42--e-=MnO4-,阴极是溶液中的氢离子放电产生氢气,所以总反应式为2K2MnO4+2H2O电解2KMnO4+2KOH+H2↑。
考点:考查反应速率计算、外界条件对反应速率的影响以及电解原理的应用
本题难度:一般
5、填空题 (9分)(1)体积相同,c(H+)相同的盐酸和醋酸溶液分别与足量的颗粒大小相同的锌粒反应,开始时产生氢气的速率 ,充分反应后产生氢气的量 (相同、醋酸的多、盐酸的多),原因是 。
(2)在一定量的盐酸溶液中加入足量的锌粒,要使产生氢气的量保持不变,但反应速率加快,可加入 晶体,理由是 ;要使产生氢气的量不变,但反应速率减慢,可加入 晶体,理由是 。
可供选择的晶体有:
A.纯碱
B.烧碱
C.胆矾
D.醋酸钠 E.KHSO4
参考答案:(1)相等 醋酸的多 当c
本题解析:略
本题难度:简单
|
|