微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 利用碳棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当碳棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗.试计算:
(1)有多少个电子通过了导线.
(2)原稀硫酸溶液的物质的量浓度.
2、选择题 下列关于原电池的叙述中,错误的是 [???? ]
A.原电池是将化学能转化为电能的装置
B.用导线连接的两种不同金属同时插入液体中,能形成原电池
C.在原电池中,电子流出的一极是负极,发生氧化反应
D.在原电池中,电子流入的一极是正极,发生还原反应
3、选择题 A、B、C都是金属,A和C分别放入同浓度的稀硫酸中,A的反应速率比C快,A与B和硫酸铜溶液组成原电池时,A的质量增加.A、B、C三种金属的活动性顺序为( )
A.A>B>C
B.A>C>B
C.B>A>C
D.C>A>B
4、选择题 镍―镉可充电电池可发生如下反应:Cd(OH)2+2Ni(OH)2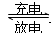 Cd+2NiO(OH)+2H2O,由此可知,该电池的负极材料是(?)
Cd+2NiO(OH)+2H2O,由此可知,该电池的负极材料是(?)
A.Cd
B.NiO(OH)
C.Cd(OH)2
D.Ni(OH)2
5、选择题 控制适当的条件,将反应2Fe3++2I-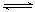 2Fe2++I2设计成如图所示的原电池。下列判断正确的是
2Fe2++I2设计成如图所示的原电池。下列判断正确的是

A.反应开始时,乙中电极反应为2I-+2e-="=" I2
B.反应开始时,甲中石墨电极上发生氧化反应
C.电流表指针为零时,两池溶液颜色相同
D.平衡时甲中溶入FeCl2固体后,乙池的石墨电极为正极