微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA- HA-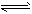 H++A2-
H++A2-
回答下列问题:
(1)Na2A溶液显____________(填“酸性”,“中性”,或“碱性”)。理由是__________________________________(用离子方程式表示)
(2)在0.1mol・L-1的Na2A溶液中,下列微粒浓度关系式不正确的是__________
A、c(A2-) +c(HA-) =0.1mol・L-1
B、c(H+) =c(OH-) +c(HA-)
C、c(Na+)+ c(H+) =c(OH-)+c(HA-)+c(A2-)
D、c(Na+) =2c(A2-) +2c(HA-)
(3)已知0.1mol・L-1NaHA溶液的pH=2,则0.1mol・L-1 H2A溶液中c(A2-)可能是_______0.11 mol・L-1
(填“<”,“>”,或“=”)理由是_________。
(4)0.1mol・L-1 NaHA溶液中各种离子浓度由大到小的顺序是____。
参考答案:(1)碱性;A2-+H2O![]() 本题解析:
本题解析:
本题难度:一般
2、选择题 已知0.1mol?L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是( ? )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
参考答案:C
本题解析:
本题难度:简单
3、选择题 有三种一元酸HA、HB、HC的钠盐分别为NaA、NaB、NaC,它们的物质的量浓度相同时,溶液的PH依次为9,10,8。则这三种弱酸的酸性由强到弱的顺序是[???? ]
A.HA>HB>HC
B.HB>HA>HC
C.HC>HB>HA
D.HC>HA>HB
参考答案:D
本题解析:
本题难度:一般
4、简答题 室温下有①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液各25mL,下列说法正确的是( )
A.物质的量浓度均为0.1mol/L,3种溶液pH的大小顺序是③>②>①
B.物质的量浓度均为0.1mol/L,将3种溶液稀释相同倍数,pH变化最大的是②
C.物质的量浓度均为0.1mol/L,分别加入25mL0.1mol/L盐酸后,pH最大的是①
D.pH均为9时,3种溶液的物质的量浓度的大小顺序是②>③>①
参考答案:A.等浓度时强碱的pH最大,强碱弱酸盐中对应的酸性越强,水解
本题解析:
本题难度:一般
5、选择题 常温下0.2 mol・ L-1 HCN和0.1 mol・L-1 NaOH等体积混合后溶液pH >7,混合溶液中有关粒子物质的量浓度关系正确的是
[?????]
A. c(HCN) +c(CN-)=c(Na+)
B. c(HCN) +2c(H+) =2c(OH-)+c(CN-)
C. c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+)
D. c(HCN)>c(CN-)>c(Na+)>c(H+)>c(OH-)
参考答案:BC
本题解析:
本题难度:一般