微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 生态农业涉及农家肥料的综合利用。某种肥料经发酵得到一种含有甲烷(CH4) 、二氧化碳、氮气的混合气体8.96L(标准状况)。该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:
CH4+CuO CO2↑+H2O↑+Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入足量的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。
CO2↑+H2O↑+Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入足量的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。
(1) 用单线桥法标明CH4+CuO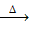 CO2↑+H2O↑+Cu电子转移的方向和数目
CO2↑+H2O↑+Cu电子转移的方向和数目
(2) 原混合气体的物质的量是____________;
(3)求原混合气体中甲烷及氮气体积。
参考答案:(1)?![]() 本题解析:
本题解析:
本题难度:一般
2、选择题 下列反应中气体只作氧化剂的是
A.Cl2通入水中
B.Cl2通入Na2SO3水溶液中
C.二氧化硫通入氯水中
D.NO2通入水中
参考答案:B
本题解析:
本题难度:困难
3、选择题 500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-) =6mol/L,用石墨做电极电解此溶液,当通电一段时间后,两极均收集到22. 4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是[???? ]
A.原混合溶液中c(K+)为2mol/L
B.上述电解过程中共转移4mol电子
C.电解得到的Cu的物质的量为0.5mol
D.电解后溶液中c(H+)为2mol/L
参考答案:AB
本题解析:
本题难度:一般
4、选择题 下列各组物质间反应,其中水既不作氧化剂又不作还原剂的氧化-还原反应是:
①Na+H2O??②Na2O2+H2O??③CO2+H2O??④Na2O+H2O??⑤Cl2+H2O???⑥NO2+H2O.
A.①③⑤
B.③④⑥
C.③⑥
D.②⑤⑥
参考答案:D
本题解析:分析:氧化还原反应中水既不作氧化剂、又不作还原剂,则水中H、O元素的化合价都不发生变化.
解答:①2Na+2H2O=2NaOH+H2↑中,水中氢元素的化合价降低,则水作氧化剂,故错误.
?②2Na2O2+2H2O=4NaOH+O2↑中,过氧化钠中氧元素的化合价既升高又降低,则过氧化钠既作氧化剂又作还原剂,
而水中H、O元素的化合价都不发生变化,则水既不作做氧化剂、又不作还原剂,故正确.
③CO2+H2O=H2CO3中,该反应中各元素的化合价都不变化,所以不是氧化还原反应,故错误.
④Na2O+H2O=2NaOH中,该反应中各元素的化合价都不变化,所以不是氧化还原反应,故错误.
⑤Cl2+H2O=HCl+HClO中,氯气中氯元素的化合价既有升高又有降低,所以氯气既作氧化剂又作还原剂,而水中H、O元素的化合价都不发生变化,则水既不作做氧化剂、又不作还原剂,故正确.
⑥3NO2+H2O=2HNO3+NO中,二氧化氮中氮元素的化合价既有升高的又有降低的,所以二氧化氮既作氧化剂又作还原剂,而水中H、O元素的化合价都不发生变化,则水既不作做氧化剂、又不作还原剂,故正确.
故选D.
点评:本题考查氧化还原反应及氧化还原反应中水的作用,明确元素的化合价变化是解答的关键,难度不大.
本题难度:简单
5、选择题 时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域。测定含I-浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度。主要步骤是
①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去
②再加入过量的碘化钾,在酸性条件下,使IO3-完全转化成I2
③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为H2N-NH2+2I2→4I-+N2↑+4H+
④将生成的I-萃取到水层后用①法处理。
⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化。
⑥将⑤反应后的溶液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:2Na2S2O3+I2→Na2S4O6+2NaI 经过上述放大后,则溶液中I-浓度放大为原溶液中I-浓度的(设放大前后溶液体积相等) [???? ]
A.2倍
B.4倍
C.6倍
D.36倍
参考答案:D
本题解析:
本题难度:一般