微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知3.2g某气体的分子数目为3.01×1022,由此推知该气体的摩尔质量是
A.64
B.32g?mol-1
C.32
D.64g?mol-1
参考答案:D
本题解析:分析:先根据气体分子数求出气体的物质的量,然后根据m=n×M求出摩尔质量.
解答:由气体分子数求气体的物质的量N=n×NA,n=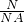 =
=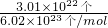 =0.05mol,
=0.05mol,
由m=n×M得M= =
=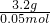 =64g/mol,
=64g/mol,
所以该分子的摩尔质量是64g/mol,
故选D.
点评:本题考查的是一个有关物质的量的小型计算,找出各物理量间的关系、灵活运用公式是解题的关键,要求学生会在基本公式的基础上进行推倒,做题时才能游刃有余.
本题难度:困难
2、选择题 下列试剂可用带玻璃塞的玻璃瓶保存的是
A.硅酸钠溶液
B.盐酸
C.氢氟酸
D.氢氧化钠溶液
参考答案:B
本题解析:分析:能和二氧化硅反应的药品溶液不能盛放在玻璃试剂瓶中,能和二氧化硅反应生成粘性物质的药品或粘性药品不能盛放在带玻璃塞的试剂瓶中.
解答:A、硅酸钠溶液具有黏性,能把玻璃塞黏住,所以不能盛放在带有玻璃塞的试剂瓶中,故A错误;
B、稀盐酸呈酸性,不和二氧化硅反应,所以可以带玻璃塞的试剂瓶盛放,故B正确;
C、氢氟酸和二氧化硅反应生成四氟化硅,所以不能用玻璃瓶盛放氢氟酸,要用塑料瓶盛放,故C错误;
D、氢氧化钠呈强碱性,能和二氧化硅反应生成硅酸钠,硅酸钠具有黏性,能把玻璃塞黏住,所以不能盛放在带有玻璃塞的试剂瓶中,故D错误;
故选B.
点评:本题以试剂的存放为载体考查了硅酸钠的性质、玻璃的成分等知识点,难度不大,试剂的存放遵循安全性、保纯性、方便性原则
本题难度:一般
3、选择题 a?mol氢气分子和a?mol氦气分子一定具有相同的
A.原子数
B.质子数
C.质量
D.体积
参考答案:B
本题解析:分析:根据m=nM、V=nVm、N(分子数)=nNA及分子的构成、一个分子中含有的质子数计算比较.
解答:A.根据N(分子数)=nNA知,物质的量相等的氢气和氦气,其分子数相等,一个氢气分子中含有2个氢原子,一个氦气分子中含有一个氦原子,所以其原子个数不等,故A错误;
B.根据N(分子数)=nNA知,物质的量相等的氢气和氦气,其分子数相等,一个氢气分子中含有2个质子,一个氦气分子中含有2个质子,所以含有的质子数相等,故B正确;
C.根据m=nM知,等物质的量的氢气和氦气,其质量与摩尔质量有关,氢气的摩尔质量是2g/mol,氦气的是4g/mol,所以其质量不等,故C错误;
D.气体摩尔体积未知,导致无法判断其体积大小,故D错误;
故选B.
点评:本题考查了阿伏伽德罗定律及推论,注意氦气是单原子分子,为易错点.
本题难度:一般
4、选择题 下列物质中含氢原子个数最多的是
A.5g H2
B.2mol H2O
C.23g C2H5OH
D.1mol NH3
参考答案:A
本题解析:分析:利用n=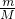 来计算物质的物质的量,再利用物质的构成来分析含有的氢原子,氢原子的物质的量越多,氢原子个数就越多.
来计算物质的物质的量,再利用物质的构成来分析含有的氢原子,氢原子的物质的量越多,氢原子个数就越多.
解答:A、氢气的物质的量为 =2.5mol,H原子的物质的量为2.5mol×2=5mol;
=2.5mol,H原子的物质的量为2.5mol×2=5mol;
B、2mol H2O中H原子的物质的量为2mol×2=4mol;
C、乙醇的物质的量为 =0.5mol,H原子的物质的量为0.5mol×6=3mol;
=0.5mol,H原子的物质的量为0.5mol×6=3mol;
D、1mol NH3中H原子的物质的量为1mol×3=3mol;
显然氢气中的氢原子的物质的量最大,则氢原子个数最多,
故选A.
点评:本题考查学生利用质量和物质的量的关系来计算,明确分子的构成是解答本题的关键,较简单,注重了对基础知识的考查.
本题难度:一般
5、选择题 为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂过滤后,再加入适量的盐酸,这种试剂是
A.NH3?H2O
B.NaOH
C.Na2CO3
D.MgCO3
参考答案:D
本题解析:分析:Fe3+易水解生成沉淀,可通过调节溶液pH的方法促进Fe3+的水解,注意不能引入新的杂质.
解答:A.加入氨水混入氯化铵杂质,且生成氢氧化镁沉淀,故A错误;
B.加入NaOH易生成氢氧化镁沉淀,且混入NaCl杂质,故B错误;
C.加入碳酸钠,易混入NaCl杂质,故C错误;
D.加入碳酸镁,与氢离子反应,可起到调节溶液pH的作用,促进铁离子的水解生成氢氧化铁沉淀而除去,且不引入新的杂质,故D正确.
故选D.
点评:本题考查物质的分离和提纯,注意根据铁离子易水解的性质用调节溶液pH的方法除杂,注意不能引入新的杂质.
本题难度:简单