��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��50mLNaOH��Һ����������ͨ��һ������CO2�����ȡ����Һϡ��.������Һ����μ���0.1mol/L��HCl��Һ��������CO2�������������������������������֮�������ͼ��ʾ��
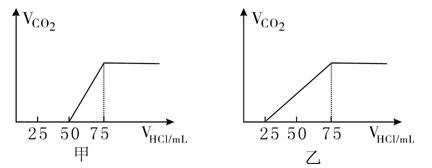
�Է���NaOH������CO2������ڼ�������Һ�д��ڵ������� ,�����ʵ���֮���� , ������CO2���������������� . ����������Һ�д��ڵ������� ,�����ʵ���֮���� , ������CO2���������������� ��
�ο��𰸣��ף�NaOH��Na2CO3��1:1��0.056 L���ң�Na
���������NaOH��Һ��ͨ��һ������CO2���м��������һ�������CO2���㣬��Ӧ��Ļ����ΪNaOH��Na2CO3����һ������Ƕ���ǡ����ȫ��Ӧ����Na2CO3�������������CO2������ȫ��NaOHת��ΪNaHCO3�������������CO2��������Ӧ��Ļ����ΪNaHCO3��Na2CO3��
������ͼ��:��������50mLʱ��ʼ����CO2���壬����Ӧ�������25mL���ᣬ���ݷ�Ӧ��
Na2CO3+HCl=NaHCO3+NaCl �� NaHCO3+HCl=NaCl+H2O+CO2����
��֪�μӵ�50 mLʱ��ʼ��Ӧ�ڣ����ݺ�������֪NaHCO3�����ʵ���������ͼ�����50mL��ǰ��������ų��������ᷴӦת��ΪNaHCO3Ӧ����25 mL���ᣬ����NaOH��Ӧ������ҲӦ��25 mL���ɴ˵�Ҳ�׳ɷ�ֻ��ΪNaOH��Na2CO3�������ʵ���֮��Ϊ1:1������CO2�����Ϊ0. 056L.

�����Ѷȣ�һ��
2��ѡ���� 25��ʱ��pH��3��CH3COOH��Һ�У���ˮ�������H+Ũ����
A.1.0��10-7 mol/L
B.1.0��10-11 mol/L
C.1.0��10-3 mol/L
D.1.0��10-14 mol/L
�ο��𰸣�B
���������pH��3��CH3COOH��Һ�У�pOH��11��ˮ�����c(OH-)��1.0��10-11��c(H+)��
�����Ѷȣ�һ��
3��ѡ���� ���е��뷽��ʽ����ȷ���ǣ�������
A��NH3?H2O?NH4++OH-
B��Ca��OH��2?Ca2++2OH-
C��HCO3-?H++CO32-
D��Al2��SO4��3�T2Al3++3SO42-
�ο��𰸣�B
���������
�����Ѷȣ���
4��ѡ���� �ڳ����£���ˮ�д��ڵ���ƽ��H2O?H++OH-����Ҫʹˮ�ĵ���̶�����ʹc��H+������Ӧ����������ǣ�������
A��NaHSO4
B��KAl��SO4��2
C��NaHCO3
D��NaAc
�ο��𰸣�A��NaHSO4=Na++H++SO42-����Һ�е������Ӷ�
���������
�����Ѷȣ���
5��ѡ���� ���ʵ���Ũ����ͬ��������Һ�У����ϰ�pH��С����˳�����е��ǣ� ��
A��Na2CO3��NaHCO3��NaCl��NH4Cl
B��NH4Cl��NaCl ��Na2CO3��NaHCO3
C��(NH4)2SO4��NH4Cl��NaNO3��Na2S
D��NH4Cl ��(NH4)2SO4��Na2S ��NaNO3
�ο��𰸣�C
���������
��������� NH4Clǿ��������ˮ��Һ�����ԣ�NaCl��ǿ��ǿ���Σ���Һ�����ԣ� Na2CO3��NaHCO3����ǿ�������Σ�ˮ��ʹ��Һ�Լ��ԣ�����Na2CO3>NaHCO3������pH��С����˳��������NH4Cl>NaCl> NaHCO3> Na2CO3�����A��B������NH4Cl��ǿ��������ˮ��Һ�����ԣ�(NH4)2SO4��ǿ��������ˮ��Һ�����ԣ���������Һ���ʵ���Ũ����ͬ��笠����ӵ�Ũ�ȣ�(NH4)2SO4>NH4Cl��笠����ӵ�Ũ��Խ��ˮ��õ���c(H+)��Խ����Һ�����Ծ�Խǿ������pH��С��ϵ��(NH4)2SO4<NH4Cl��NaNO3��ǿ��ǿ���Σ���Һ�����ԡ�Na2S��ǿ�������Σ�ˮ��ʹ��Һ�Լ��ԡ�����pH��С����˳�����е���(NH4)2SO4<NH4Cl< NaNO3<Na2S�����C��ȷ��D����
���㣺������ˮ���ڱȽ�����Һ��pH�Ĵ�СӦ�õ�֪ʶ��
�����Ѷȣ�һ��