微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是(??)
A.非金属元素R所形成的含氧酸盐(NaROb)中的R元素必定呈现正价
B.只有非金属能形成含氧酸或含氧酸盐
C.除稀有气体外的非金属元素都能生成不同价态的含氧酸
D.非金属的最高价含氧酸都具有强氧化性
参考答案:A
本题解析:
试题分析:A. 在任何化合物中正负化合价的代数和为0.因为O的化合价是负价,Na的化合价为+1价,所以非金属元素R所形成的含氧酸盐(NaROb)中的R元素必定呈现正价。正确。B.非金属和金属元素都可以形成含氧酸或含氧酸盐。如H2CO3、Na2CO3;HMnO4、KMnO4等。错误。C. 有些非金属元素如O、F由于非金属性很强,不能生成不同价态的含氧酸。错误。D.不是所有的非金属的最高价含氧酸都具有强氧化性。如H2CO3、H3PO4无强氧化性。错误。
本题难度:一般
2、选择题 在一集气瓶充入
1
2
体积H2,1
4
体积N2,1
4
体积Cl2,光照使之爆炸后,倒置于水槽中,最后进入集气瓶中的水的体积应该是( )
A.1
3
体积
B.1
4
体积
C.1
2
体积
D.2
3
体积
参考答案:集气瓶充入12
本题解析:
本题难度:一般
3、填空题 组同学发现84消毒液与洁厕剂(主要成分为盐酸)室温下混和有Cl2生成,于是尝试在实验室利用该反应原理制取Cl2。
(1)若用次氯酸钙、浓盐酸为原料,利用下图装置制取Cl2。装置中仪器a的名称为 ??????。甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,有无色气泡产生。乙同学认为不合理,理由是????????????。又知:室温下H2CO3的电离常数K1=4.2×10-7,K2=5.6×10-11,则pH为8.0的NaHCO3溶液中[CO32-]:[HCO3-]=???????。

(2)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如下装置制备无水FeCl3。
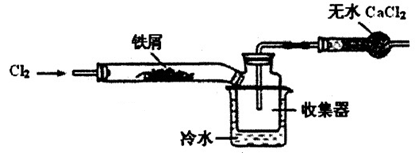
①下列操作步骤的正确排序为????????(填字母)。
A.体系冷却后,停止通入Cl2
B.通入干燥的Cl2赶尽装置中的空气
C.在铁屑下方加热至反应完成
D.用干燥的H2赶尽Cl2
E.检验装置的气密性
②该实验装置存在的明显缺陷是?????????????????。
(3)世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂。
已知:NaCl+3H2O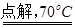 NaClO3+3H2 NaClO3+3H2 , ,
2NaClO3+4HCl=2C1O2 +Cl2 +Cl2 +2NaCl+2H2O。 +2NaCl+2H2O。
有关物质性质:
物质
| 熔点/℃
| 沸点/℃
| C1O2
| -59
| 11
| Cl2
| -107
| -34.6
?
ClO2的生产流程示意图:
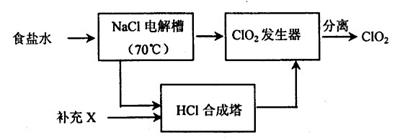
该工艺中,需要补充的物质X为???(填化学式),能参与循环的物质是??????(填化学式)。从ClO2发生器中分离出ClO2可采用的方法是????????????。
参考答案:(1)分液漏斗(2分)
制取的氯气中含有HCl气体,H
本题解析:
试题分析:(1)根据实验装置图可知仪器a为分液漏斗;因为浓盐酸具有挥发性,制取的Cl2中含有HCl,HCl溶于水后能与NaHCO3反应产生CO2气体;HCO3?电离产生CO32?:HCO3?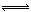 CO32?+H+,K2=[CO32?][H+]/[HCO3?]=5.6×10-11, 可得[CO32-]:[HCO CO32?+H+,K2=[CO32?][H+]/[HCO3?]=5.6×10-11, 可得[CO32-]:[HCO
本题难度:一般
4、选择题 下列有关氯气的叙述中,正确的是(???)
A.工业上常用MnO 2和稀盐酸共热来制取氯气 2和稀盐酸共热来制取氯气
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.在氧化还原反应中,Cl2只能作氧化剂
D.若含0.4 mol HCl的浓盐酸,MnO2过量,可制得标准状况下氯气2.24 L
参考答案:B
本题解析:略
本题难度:简单
5、选择题 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合不可能是下列的( )
A.亚硫酸钠溶液、氯气
B.水、二氧化氮
C.氢氧化钠溶液、一氧化氮
D.氢氧化钠溶液、氨气

参考答案:A、亚硫酸钠溶液能吸收氯气,发生反应,打开夹子时①中的气体进
本题解析:
本题难度:一般
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772
|
|
|
|
|