��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ����ͭ����пƬ��200mlϡ�������ԭ��أ�����ѧ��ת��Ϊ���ܣ���ͭ���Ϲ�����3��36L����״��������ʱ������ǡ��ȫ�������ġ���ش��������⣺
��1����ԭ��ص�������ӦʽΪ��______________________
��2������ԭϡ��������ʵ���Ũ�ȡ�
��3������ͭ��������Ƭ���������ʽ����������ܷ����ԭ����أ�__________����ܡ����ܡ��� �������ԭ��أ���ԭ��صĸ�����Ӧʽ��_____________________
�ο��𰸣���1��2H++2e-==H2��
��2��0.75mol/
���������
�����Ѷȣ�һ��
2��ѡ���� ���з����У��ܹ�ʹ��ӦCu+2H2O�TCu��OH��2��+H2���������ǣ�������
A��ͭƬ��ԭ��صĸ�����̼����ԭ��ص��������Ȼ������������Һ
B��ͭп�Ͻ��ڳ�ʪ�Ŀ����з����绯ѧ��ʴ
C����ͭƬ���������缫�������������Һ
D����ͭƬ���������缫���������ͭ��Һ
�ο��𰸣�����ͭ��ˮ֮�䷢���ķ�Ӧ�Ƿ��Է���������ԭ��Ӧ��Ӧ��Ƴɵ��
���������
�����Ѷȣ���
3������� ����10�֣���������һ����Ҫ�����ȼ�ϣ�Ҳ�������������������ȣ��Գ��������ƻ����á���ҵ�Ͽ����ý�̿��ˮ�����ڸ����µķ�Ӧ���ˮú�����ϳɶ����ѡ���ش��������⣺
��1������ˮú������Ҫ��ѧ��Ӧ����ʽΪ������������������������������������������
��2����ú�����������в������к�����H2S��Na2CO3��Һ���գ�����������ʽ�Σ��÷�Ӧ�Ļ�ѧ����ʽΪ��������������������������������������������������������
��3��������ˮú���ϳɶ����ѵ�������Ӧ���£�
������ 2H2(g)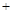 CO(g)
CO(g) CH3OH(g)
CH3OH(g)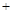 90.8 kJ
90.8 kJ
������ 2CH3OH(g) CH3OCH3(g)
CH3OCH3(g)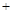 H2O(g)
H2O(g)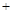 23.5 kJ
23.5 kJ
������ CO(g)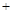 H2O(g)
H2O(g) CO2(g)
CO2(g)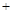 H2(g)
H2(g)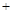 41.3 kJ
41.3 kJ
�����ܷ�Ӧ��3H2(g)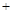 3CO(g)
3CO(g) CH3OCH3(g)
CH3OCH3(g)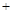 CO2(g)
CO2(g)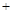 Q������Q
Q������Q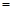 ����������kJ��
����������kJ��
����һ�������µ��ܱ������У����ܷ�Ӧ�ﵽƽ�⣬Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��
����������������ĸ���ţ���
a�����¸�ѹ??????????????? b���������??????????? c������CO2��Ũ��???? d������CO��Ũ��
��4������֪ij�¶��·�Ӧ��2CH3OH(g) CH3OCH3(g)
CH3OCH3(g)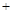 H2O(g)��һ�ܱ������н��е�10minʱǡ�ô�ƽ�⣬��ø���ֵ�Ũ�����£�
H2O(g)��һ�ܱ������н��е�10minʱǡ�ô�ƽ�⣬��ø���ֵ�Ũ�����£�