微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)

已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇水会强烈水解生成H3PO3和HCl,遇O2会生成POCl3,POCl3溶于PCl3。PCl3、POCl3的熔沸点见下表:
物质
| 熔点/℃
| 沸点/℃
|
PCl3
| -112
| 75.5
|
POCl3
| 2
| 105.3
?
请回答下列问题:
(1)A装置中制氯气的离子方程式为 。?
(2)B中所装试剂是 ,E中冷水的作用是 ,F中碱石灰的作用是 。?
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通入干燥CO2的作用是 。通过控制K1、K2能除去A、B装置中的空气,具体的方法是 。?
(4)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过 (填实验操作名称),即可得到较纯净的PCl3。?
参考答案:(1)MnO2+4H++2Cl- 本题解析:(2)评价成套装置最后的仪器作用一般从两个方面考虑:①尾气处理;②防止空气干扰;(3)注意除去A、B装置中的空气,无法用CO2除,只能用生成的Cl2来排除;(4)依据信息“POCl3溶于PCl3,PCl3、POCl3的熔沸点”可知分离混合物的方法 本题解析:(2)评价成套装置最后的仪器作用一般从两个方面考虑:①尾气处理;②防止空气干扰;(3)注意除去A、B装置中的空气,无法用CO2除,只能用生成的Cl2来排除;(4)依据信息“POCl3溶于PCl3,PCl3、POCl3的熔沸点”可知分离混合物的方法
本题难度:一般
2、实验题 请你设计至少两种方法除去细小的铁颗粒中混有的细小的铝颗粒。(简要说明)
_______________________________________________
参考答案:方法一:可以使用NaOH溶液洗涤混合物,铁与NaOH溶液不发
本题解析:
本题难度:一般
3、选择题 能够鉴定1―氯丙烷中存在氯元素的操作是
A.在1―氯丙烷中直接加入AgNO3溶液
B.将1―氯丙烷溶于水,然后加入AgNO3溶液
C.在1―氯丙烷中加入NaOH溶液,加热再用硝酸酸化,然后加入AgNO3溶液
D.在1―氯丙烷中加入乙醇,加热再用盐酸酸化,然后加入AgNO3溶液
参考答案:C
本题解析:略
本题难度:简单
4、填空题 工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
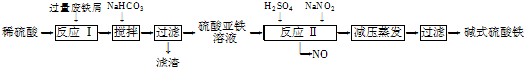
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物
| Fe(OH)3
| Fe(OH)2
| Al(OH)3
| 开始沉淀
| 2.3
| 7.5
| 3.4
| 完全沉淀
| 3.2
| 9.7
| 4.4
?
回答下列问题:
(1)反应Ⅰ中发生的氧化还原反应的化学方程式为??????????????????????????。
(2)加入少量NaHCO3的目的是调节pH,使溶液中的________(填“Fe3+”、“Fe2+”或“Al3+”)沉淀。该工艺流程中“搅拌”的作用是______________________。
(3)反应Ⅱ的离子方程式为??????????????????????????___。在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作____?????____。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为____________________________。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液
参考答案:(1) Fe + Fe2(SO4)2 = 2FeSO4
本题解析:
试题分析:(1)根据题意及流程图分析知,反应Ⅰ中发生的反应为Al2O3+3H2SO4=Al2(SO4)3+3H2O,Fe2O3+3H2SO4= Fe2(SO4)2+3H2O, Fe + Fe2(SO4)2 = 2FeSO4,Fe +H2SO4(稀)=FeSO4+H2↑,其中属于氧化还原反应的为Fe + Fe2(SO4)2 = 2FeSO4,(Fe +H2SO4(稀)=FeSO4+H2↑);(2)根据题意及流程图分析知,反应Ⅰ后溶液的成分为硫酸亚铁和硫酸铝的混合溶液,经搅拌、过滤后得硫酸亚铁溶液,所以加入少量NaHCO3的目的是调节pH,使溶液中的Al3+沉淀。该工艺流程中“搅拌”的作用是加快反应速率;(3)由题给信息知,反应Ⅱ中NaNO2中氮元素的化合价由反应前的+3价降为反应后NO中的+2,则硫酸亚铁中铁元素的化合价必然升高,由Fe2+转化为Fe3+,反应的离子方程式为Fe2+ + NO2- + 2 H+ = Fe3+ + NO↑ + H2O,反应Ⅱ的目的是利用氧化剂将Fe2+氧化为Fe3+,O2与NaNO2在反应中做氧化剂;n(O2)=0.5mol,则得到电子0.5mol×4=2mol,1molNaNO2被还原生成NO,化合价由+3价降低到+2价,得到1mol电子,根据得失电子数目相等知,节约NaNO2的物质的量为 2mol;(4)[Fe(OH)]2+离子,可部分水解生成[Fe2(OH)4]2+聚合离子,根据电荷守恒和质量守恒可写出反应的离子方程式为
2[Fe(OH)]2++2H2O=[Fe2(OH)4]2++2H+;(5)A、氯水可以氧化亚铁离子为铁离子,溶液颜色变化不明显,不能检验亚铁离子,错误;B、KSCN溶液和亚铁离子混合无现象发生,不能检验亚铁离子,错误;C、NaOH溶液加入和铁离子反应生成红褐色沉淀不能检验是否存在亚铁离子,错误;D、在含有Fe3+的溶液中检验Fe2+,应选用酸性KMnO4溶液,现象明显,酸性KMnO4溶液氧化亚铁离子高锰酸钾溶液褪色,正确,选D。
本题难度:困难
5、选择题 从碘的四氯化碳溶液中分离出碘、并回收四氯化碳,所采用的方法是
A.蒸发
B.蒸馏
C.过滤
D.分液
参考答案:B
本题解析:略
本题难度:简单
|
|