饱和NaHSO3溶液
参考答案:C
本题解析:
试题分析:碳酸钠和碳酸氢钠均可与澄清石灰水反应,A错误;氯化亚铁溶液、氯化铁溶液均能与氢氧化钠溶液反应,B错误;铝与氢氧化钠溶液反应而铁与氢氧化钠溶液不反应,C正确;饱和亚硫酸氢钠溶液与二氧化硫不反应,D错误。
点评:除去碳酸钠固体中的碳酸氢钠,可用加热法;除去碳酸钠溶液中的碳酸氢钠,可加适量氢氧化钠溶液;除去氯化亚铁溶液中氯化铁可加过量铁粉;除去二氧化碳中二氧化硫气体可用饱和碳酸氢钠溶液。
本题难度:一般
2、选择题 下列物质可用重结晶法提纯的是
A.含杂质的工业酒精
B.含杂质的粗苯甲酸
C.从溴水中提纯溴
D.苯中混有少量苯酚
参考答案:B
本题解析:略
本题难度:简单
3、选择题 下列关于0.2mol/L的Ba(NO3)2溶液不正确的说法是
A.500mL溶液中NO3-物质的量为0.2NA
B.500mL溶液中NO3-离子浓度为0.4mol/L
C.500mL溶液中Ba2+离子浓度为0.2mol/L
D.1L溶液中阴、阳离子总数为0.8NA
参考答案:AD
本题解析:分析:A、根据n(NO3-)=2c(Ba(NO3)2)V计算;
B、根据溶液中离子的物质的量浓度=化学式中离子个数×溶液的物质的量浓度计算;
C、根据溶液中离子的物质的量浓度=化学式中离子个数×溶液的物质的量浓度计算;
D、根据N=化学式中阴阳离子个数×c(Ba(NO3)2)VNA计算.
解答:A、n(NO3-)=2 c(Ba(NO3)2)V=2×0.2mol/L×0.5L=0.2mol,故A错误;
B、C(NO3-)=2×c(Ba(NO3)2)=2×0.2mol/L=0.4mol/L,故B正确;
C、C(Ba2+)=1×c(Ba(NO3)2)=1×0.2mol/L=0.2mol/L,故C正确;
D、N(阴阳离子数)=3×c(Ba(NO3)2)V NA=3×0.2mol/L×1L×NA=0.6NA,故D错误;
故选AD.
点评:本题考查了有关物质的量浓度的计算,难度不大,明确化学式与离子的关系是解本题的关键.
本题难度:困难
4、选择题 化学实验中常将某些溶液或试剂进行酸化或碱化。下列处理中正确的是(?? )
A.检验KClO3中的氯元素,可加入AgNO3和稀硝酸
B.为提高KMnO4溶液的氧化能力,用浓盐酸将KMnO4溶液酸化
C.检验蔗糖在稀硫酸中水解产生的葡萄糖,应先用NaOH溶液碱化后才能进一步检验
D.检验溶液中是否含有SO42-时,先加氯化钡溶液后,再加稀盐酸酸化
参考答案:C
本题解析:KClO3中的氯元素以ClO3-的形式存在,无单个的Cl-,不能用AgNO3检验,A选项错误;为提高KMnO4溶液的氧化能力,用硫酸酸化,选项B 错误;检验溶液中是否含有SO42-时,先加稀盐酸酸化,排除银离子、碳酸根离子等的干扰,再加氯化钡溶液,选项D错误。
本题难度:一般
5、选择题 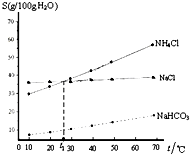 如图是NaCl、NH4Cl和NaHCO3的溶解度曲线,下列说法不正确的是 如图是NaCl、NH4Cl和NaHCO3的溶解度曲线,下列说法不正确的是
A.分别将70℃时的NH4Cl?和NaCl饱和溶液降温至40℃,析出的NH4Cl晶体质量大于NaCl晶体
B.t1℃时,饱和NaCl?和NH4Cl?溶液的质量分数相同
C.t1℃时,饱和NaCl?和NH4Cl?溶液的物质的量浓度相同
D.工业上制纯碱最关键的转化是向饱和的NaCl?溶液中通入NH3和CO2,有NaHCO3?固体析出.是因为NaHCO3?在水中的溶解度不大且比NaCl?和NH4Cl的溶解度小很多
参考答案:C
本题解析:分析:A、依据题干溶解度曲线分析判断;
B、依据题干溶解度曲线分析判断,氯化铵和氯化钠在t1℃时,溶解度相同;
C、依据题干溶解度曲线分析判断,氯化铵和氯化钠在t1℃时,溶解度相同,质量分数相同,但溶质摩尔质量不同,物质的量浓度不同;
D、图象分析得到:NaHCO3?在水中的溶解度不大且比NaCl?和NH4Cl的溶解度小很多.
解答:A、分别将70℃时的NH4Cl?和NaCl饱和溶液降温至40℃,依据图象变化分析,依据溶解度概念是一定温度下,100克水中达到饱和时溶解的溶质质量,所以析出的NH4Cl晶体质量大于NaCl晶体,故A正确;
B、t1℃时,氯化钠和氯化铵的溶解度相同,所以饱和溶液中溶质质量分数相同,饱和NaCl?和NH4Cl?溶液的质量分数相同,故B正确;
C、t1℃时,氯化钠和氯化铵的溶解度相同,所以饱和溶液中溶质质量分数相同,饱和NaCl?和NH4Cl?溶液的质量分数相同.但溶质摩尔质量不同,溶质物质的量不同,所以饱和NaCl?和NH4Cl?溶液的物质的量浓度不相同,故C错误;
D、结合图象中的溶解度曲线饱和可知,在水中的溶解度不大且碳酸氢钠溶解度比NaCl?和NH4Cl的溶解度小很多,向饱和的NaCl?溶液中通入NH3和CO2,有NaHCO3?固体析出,故D正确;
故选C.
点评:本题考查了从溶解度曲线图上读取信息、分析及获取信息的能力,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;温度对不同物质的溶解度影响情况.关键是溶解度概念和饱和溶液的组成特征.
本题难度:一般
|