��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��16�֣���ȸʯ��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4��5H2O��CaCO3���������£�

�Իش��������⣺
��1����δ����H2O2����ҺA�У����ڵĽ���������Cu2+��Fe2+��Fe3+�����������Һ��Fe3+��ѡ������ʵ��Լ���?����?������ţ���
A��KMnO4��Һ
B��Fe��
C��Na2CO3��Һ
D��KSCN��Һ
����ҺA�м���H2O2��H2O2�ڸ÷�Ӧ������������ʵ����ѡ��H2O2������Cl2���������������ǻ��������⣬��һԭ���Dz��������������������ӡ�
��2������ҺC���CuSO4��5H2O����Ҫ��������Ũ����???�����������˵Ȳ��������ձ���©���⣬���˲��������õ���һ�����������������ڴ˲����е���Ҫ������������������
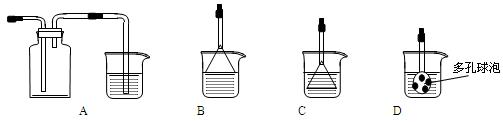
��3���Ʊ�CaCO3ʱ��������Ӧ�Ļ�ѧ����ʽ��?������������������������������?����ʵ��������а����ݳ�����ѡ������װ���е�?����?������ţ�װ�����հ�����
���ձ��е�Һ�嶼Ϊˮ��
��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ�������100 mL 0.1 mol�MLKMnO4����Һ�����Ƹ���Һʱ�����ձ�������������ͷ�ι��⣬�����һ�ֲ���������??����������???�������ò��������м�����ˮ���ӽ��̶���1��2cmʱ��Ӧ�������������������μ�����ˮ����Һ�İ�Һ��������̶�����ƽ��
�ο��𰸣���ÿ��2�֣���16�֣�
��1��D������Cl��
��
�����������
�����Ѷȣ�һ��
2��ʵ���� ��10�֣�����ʵ�顱����װ�ü����������ŵ㣬���ͼʾ�ش��й�����
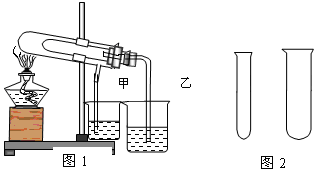
��1��������ͼ1�Ƚ�̼�����ƺ�̼���Ƶ����ȶ��ԣ�������ֽ������Ӧ�ڴ��Թܵײ�����??????????���ѧʽ����ʯ��ˮ����ǵ��ձ���??????(��ס���) ��
��д���Թ��з�Ӧ�Ļ�ѧ��Ӧ����ʽ��??????????????????????????????????????
��2��ʹ��ͼ2�д�С��һ���Թܣ������ۺ�����������Һ��ȡ���������ռ�һ�Թ�������
�����ۺ�����������Һ����??�Թ���(���С)��ɷ���װ�ã���д���÷�Ӧ������
����ʽΪ��???????????????????????????????????Ϊ��ʹ�����ռ��������ܽ�
�����س������ռ��������Թܣ�Ӧ��β�����д�����µIJ��裺???????????????????
?????????????????????????????????????????????????????????????????????????��
�ο��𰸣���1��Na2CO3����?��? 2NaHCO3 ==? Na2
�����������1��̼���Ʊ�̼�������ȶ������ԣ����Թ��ڼ���̼���ƣ�С�Թ��ڼ���̼�����ƣ�̼���������ȷֽ⣬��̼�������Ȳ��ֽ⣬���ԣ�ʯ��ˮ����ǵ��ձ����ҡ��Թ��з�Ӧ�Ļ�ѧ��Ӧ����ʽ��2NaHCO3 ?Na2CO3 + H2O + CO2��
?Na2CO3 + H2O + CO2��
��2�������ۺ�����������Һ��ȡ���������ռ�һ�Թ������������ۺ�����������Һ����С�Թ��ڣ���ɷ���װ�ã��÷�Ӧ�����ӷ���ʽΪ��2Al? +2OH�� + 2H2O =2AlO2�� + 3H2��
Ϊ��ʹ�����ռ��������ܽϴ����س������ռ��������Թܣ�Ӧ��β��������µIJ����ǣ���С�Թ�������Թܵײ�����С�Թ��г��������������������Թܡ�
�����Ѷȣ���
3��ʵ���� ��10�֣���ͼΪijʵ��С���ͬѧ�Ʊ���ϩ����֤��ϩ���ʵIJ���װ��ͼ����ش�
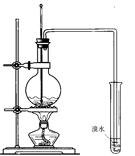
��1����ƿ�м���������Լ���__________________________��
��2���¶ȼƵ�������____________________�����Ƭ��������_________________________��
��3��д��ʵ���в�����ϩ�Ļ�ѧ����ʽ��_____????? __��
��4����ͬѧ��Ϊ����ˮ��ɫ��������֤����ϩ���в������ԣ���ԭ������ƿ��Һ����غ�ɫ������_____________���塣��ͬѧ������ϸ�۲����Ϊ���Թ�����һ�������֤����ϩ���в������ԣ����������?????????? ________________����ͬѧΪ��֤��һ��Ӧ�Ǽӳɶ�����ȡ��������˽������������պ���pH��ֽ�����Է�Ӧ����Һ�����ԣ�������____________________________________��
��5����������ʵ������ƿ�ڷ�Һ����ȷ������_______________��
A����Һֱ�ӵ�����ˮ��
B����Һ����շ�Һ����
C����ˮ������ƿ��
D����Һ����ʢ��ˮ������Ͱ�У����������ٵ�����ˮ��
�ο��𰸣���1���Ҵ���Ũ�����2�����Ʒ�Ӧ�¶���170�棬��ֹ���У�
�����������1��ʵ������ȡ��ϩ�������Ҵ���Ũ����������·�����ȥ��Ӧ�����ġ�
��2���Ҵ�������ȥ��Ӧ������ϩ�ķ�Ӧ�У��¶ȱ��������170�棬�����¶ȼƵ������ǿ��Ʒ�Ӧ�¶���170�档Ϊ�˷�ֹҺ������ʱ������������Ҫ�������Ƭ��ֹ���С�
��3������ʽΪCH3CH2OH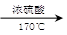 CH2==CH2��+H2O
CH2==CH2��+H2O
��4������Ũ���������ˮ�Ժ�ǿ�����ԣ�����ڷ�Ӧ��Ũ��������Ҵ���������������ԭ����SO2���壬SO2���л�ԭ�ԣ���ʹ��ˮ��ɫ����ϩ��ʹ��ˮ��ɫ������������ˮ����״�����ɣ���֤����ϩ���в������ԣ��ܺ���ˮ�����ӳɷ�Ӧ���������ȡ����Ӧ�����Ȼ�����廯�⣬�廯������ˮ�����ԡ�����Һ���Խ���������ǿ���ʿ���pH��ֽ��֤��
��5����Һ�к���Ũ���ᣬ����ѡ��D����ȷ�ģ���ѡD��
�����Ѷȣ�һ��
4��ʵ���� (5��)��ͼ��ʵ���ҳ��õ���ȡ�����װ��
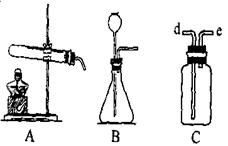
(1)����Bװ����ȡ����ʱ��ѧ����ʽ��??????????????????????????????
(2)Cװ����;�ܶ࣬������ϴ������Ҫ��ȥO2��������CO2���õ���װ�ã���ʱƿ��ʢ??????????���ѧʽ����Һ��������??????��??????������d��e����ͬ�������ſ������ռ�������ƿ��Ϊ��������������?????��?????����
�ο��𰸣���2H2O2=2H2O+O2��(������MnO2)
��N
���������
���������Bװ���ǵ��͵Ĺ�Һ�����������壬���Ʊ������ķ�Ӧ�У�ֻ�й�������Ĵ��ֽ⣬��˷���ʽΪ2H2O2=2H2O+O2��(������MnO2)��(2)CO2�����������Ҫ������CO2Ӧ����NaOH��Cװ�ó����̳�����ϴ����������d��e�����ſ������ռ�����Ӧ���������ſ�������Cװ�ö̽�����Ϊ�����ſ�������������e��d����
������������һ���dz��ȵ�Ҳ�Ƿdz�������ʵ���������ʹ���⡣Aװ���ǵ��͵Ĺ̹̼����Ʊ������װ�ã�Bװ���ǵ��͵Ĺ�Һ�������Ʊ������װ�ã�Cװ������;�㷺�����װ��Һ�壬���̳���ϴ�����̽���������ˮ�������������װ��Һ�壬���̳��������ſ������������̽������������ſ�����������
�����Ѷȣ�һ��
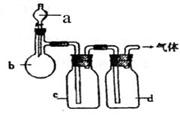
5��ѡ���� ����ͼװ����ȡ���е����ָ�����������壨ͼ������̨�����С����ȼ������ռ�װ�þ�����ȥ����Ҫʱ���Լ��ȣ�a��b��c��d��ʾ��Ӧ�����м�����Լ�����������ȷ���ǣ�???��
ѡ��
| ����
| a
| b
| c
| d
|
A
| CO2
| ����
| CaCO3
| ����Na2CO3��Һ
| Ũ����
|
B
| Cl2
| Ũ����
| MnO2
| NaOH��Һ
| Ũ����
|
C
| NH3
| ����NH4Cl��Һ
| ��ʯ��
| H2O
| ����NaOH
|
D
| NO
| ϡ����
| ͭм
| H2O
| Ũ����
�ο��𰸣�D
���������
�����������������̼�����е��Ȼ�������Ӧͨ������̼��������Һ�������ñ���̼������Һ����̼������Һ���������̼���巴Ӧ��Na2CO3+CO2+H2O=2NaHCO3����A����ȥ�����е��Ȼ��ⲻ��������������Һ��������Ҳ��������������Һ��Ӧ��Ӧ������ͨ�뱥��ʳ��ˮ�������ڱ���ʳ��ˮ���ܽ��С��B����������������ˮ������ͨ��ˮ�н���ˮ���գ�������ˮ��ȥ�����е�ˮ�������ɸ��ü�ʯ�����գ������ӷ����Ƶõ�NO�����п��ܻ���HNO3���壬����ˮ��ȥNO�е�HNO3����������Ũ������D��ȷ��
��������ϰ��ѧ��ѧ�������壨O2��H2��NH3��CO2��SO2��NO2��NO��Cl2��C2H4��C2H2�ȣ����Ʊ�ԭ����װ�á�����������ռ���
�����Ѷȣ�һ��
|