微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (11分)测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示.
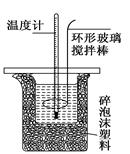
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol): ;
(2) 装置图中碎泡沫塑料所起作用为: ;
(3) ①取50 mL NaOH溶液和30 mL硫酸溶液进行实验,
实验数据如下表.请填写下表中的空白:
温度
实验次数
| 起始温度T1/℃
| 终止温度T2/℃
| 温度差平均值(T2-T1)/℃
|
H2SO4
| NaOH
| 平均值
|
1
| 26.2
| 26.0
| 26.1
| 30.1
| ________
|
2
| 27.0
| 27.4
| 27.2
| 33.3
|
3
| 25.9
| 25.9
| 25.9
| 29.8
|
4
| 26.4
| 26.2
| 26.3
| 30.4
②若上述实验所测中和热数值偏小,产生偏差的原因可能是( )
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
参考答案:(1) 本题解析: 本题解析:
试题解析:(1)稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,稀硫酸和氢氧化钠稀溶液分别是强酸、强碱,则反应的热化学方程式为:NaOH(aq)+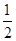 H2SO4(aq) H2SO4(aq)
本题难度:一般
2、选择题 “即食即热型快餐”适合外出旅行时使用,其内层是用铝箔包裹的并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线使两种化学物质反应,放出的热量便可对食品进行加热,这两包物质最合适的选择是(???)
A.Ba(OH)2・8H2O和NH4Cl
B.生石灰和水
C.熟石灰和水
D.食盐和水
参考答案:B
本题解析:“即食即热型快餐”是利用物质溶解放热或者化学反应放热对食品进行加热。A选项两物质反应吸热,B选项两物质反应放热,C、D两选项两物质混合时热效应不明显。故B选项符合题意。
本题难度:简单
3、选择题 某溶液中大量存在5种离子:NO3-、SO42-、Fe3+、H+、M其物质的量之比为n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,则M可能为
A.Fe2+
B.Mg2+
C.Cl-
D.Ba2+
参考答案:B
本题解析:分析:n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,由电荷守恒可知,M为阳离子,结合离子的共存来解答.
解答:n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,
2×1+3×2>1×3+3×1,由电荷守恒可知,M为阳离子,设电荷数为x,则
2×1+3×2=1×3+3×1+x×1,解得x=2,
又NO3-、Fe2+、H+发生氧化还原反应,则不能共存,则M为Mg2+,
故选B.
点评:本题考查离子的共存,注意利用电荷守恒分析M是解答本题的关键,离子之间的氧化还原反应为解答的难点,题目难度中等.
本题难度:简单
4、选择题 某无色酸性溶液中,可以大量存在的是
A.K+、Na+、CO32-、Cl-
B.K+、Na+、NO3-、HCO3-
C.Na+、K+、Cl-、SO42-
D.MnO4-、Na+、Cl-、SO42-
参考答案:C
本题解析:分析:无色酸性溶液含大量的H+,根据离子之间不能结合生成水、气体、沉淀、弱电解质等,则不能共存,并结合离子的颜色来解答.
解答:A.因H+、CO32-结合生成水和气体,则不能共存,故A错误;
B.因H+、HCO3-结合生成水和气体,则不能共存,故B错误;
C.该组离子之间不反应,且均为无色,故C正确;
D.该组离子之间不反应,能共存,但MnO4-为紫色,与无色溶液不符,故D错误;
故选C.
点评:本题考查离子的共存,侧重复分解反应发生的条件的考查,熟悉常见物质的状态、溶解性即可解答,题目难度不大.
本题难度:一般
5、选择题 当压力达到220 atm、温度达到374 ℃时,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。下列说法不正确的是( )
A.二氧化碳与超临界水作用生成汽油的反应属于放热反应
参考答案:
本题解析:
本题难度:一般
|