微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (7分)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,
用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
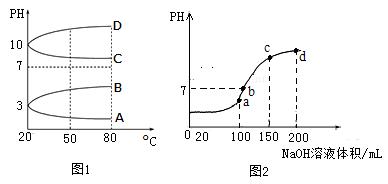
(1)相同条件下,相等物质的量浓度的NH4Al(SO4)2中c(NH4+) (填“=”、“>”“<”)NH4HSO4中c(NH4+)。
(2)如图1是0.1mol?L
参考答案:
本题解析:
本题难度:困难
2、选择题 浓度为0.1 mol/L的某物质的水溶液,且pH=5.1,则此物质应是下列中的
A.H2SO4
B.NH4Cl
C.NaHCO3
D.CH3COONa
参考答案:B
本题解析:只有A选项和B选项显酸性,但是A选项不符合pH=5.1的条件.
本题难度:困难
3、选择题 25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.1 L 0.1 mol・L-1 (NH4)2Fe(SO4)2・6H2O溶液中:c(NH4+)+c(Fe2+)+c(H+)=c(OH-)+c(SO42-)
B.0.1 mol・L-1的NH4Cl与0.1 mol・L-1的NH3・H2O等体积混合:c(NH4+)+2c(H+)=c(NH3・H2O)+2c(OH-)
C.pH=9.4、浓度均为0.1 mol・L-1的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-)
D.0.1 mol・L-1 CH3COONa 溶液与0.05 mol・L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
参考答案:BD
本题解析:
试题分析:根据电荷守恒可以判断A错误;根据电荷守恒和物料守恒可知B正确;pH=9.4说明水解大于电离,所以c(HCN) 的浓度大于c(CN-)故C错误;0.1 mol・L-1 CH3COONa 溶液与0.05 mol・L-1盐酸等体积混合后溶液中有CH3COOH为0.025mol・L-1、CH3COONa为0.025mol・L-1所以有c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)故D正确。
考点:溶液中微粒的浓度的大小比较
本题难度:困难
4、填空题 (6分)(1)硫化钠水溶液显碱性的原因_______________(用离子方程式表示)
(2)用硫化亚铁作沉淀剂除去污水中的Cu2+_______________________
(3)浑浊的石灰水中存在的溶解平衡________________
参考答案:(1)S2-+H2O 本题解析:
本题解析:
试题分析:(1) 硫化来源:91考试 网钠是强碱弱酸盐,水解显碱性,水解离子方程式为S2-+H2O HS-+OH-(2)根据沉淀转化原理:溶解度小的可以转化为溶解度更小的沉淀,方程式为:Cu2++FeS= CuS+Fe2+(3)Ca(OH)2是微溶物,存在的溶解得平衡是:Ca(OH)2(S)
HS-+OH-(2)根据沉淀转化原理:溶解度小的可以转化为溶解度更小的沉淀,方程式为:Cu2++FeS= CuS+Fe2+(3)Ca(OH)2是微溶物,存在的溶解得平衡是:Ca(OH)2(S) Ca2+ (aq)+2OH-(aq)
Ca2+ (aq)+2OH-(aq)
考点:水解,溶解平衡方程式的书写。
本题难度:一般
5、填空题 (16分)根据题给信息,完成下列各小题:
Ⅰ、某造纸厂排出的废水,经取样分析其中除了含有游离汞、纤维素以及其它的有机物外,其它成分为c(Na+)=4×10―4mol/L,c(SO42―)=2.5×10―4mol/L,c(Cl―)=1.6×10―5 mol/L,c(NO3―)=1.4×10―5 mol/L,c(Ca2+)=1.5×10―5 mol/L,则该废水的pH为________。
Ⅱ、有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大;NaA溶液呈中性;1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC分别作导电性试验,发现后者的导电性比前者强,则这四种酸的酸性由强到弱的顺序为______________________。
Ⅲ、常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得
溶液的pH如下表:
实验编号
| HA物质的量浓度(mol/L)
| NaOH物质的量浓度(mol/L)
| 混合溶液的pH
|
①
| 0.1
| 0.1
| pH=9
|
②
| c
| 0.2
| pH=7
|
③
| 0.2
| 0.1
| pH<7
请回答:
(1)从①组情况分析,HA是强酸还是弱酸__________(填“强酸”或“弱酸”);
(2)①组实验所得混合溶液中由水电离出的c(OH-)=__________mol・L-1。
(3)②组情况表明,c__________0.2 mol/L(选填“大于”、“小于”或“等于”)。
混合液中离子浓度c(A-)与c(Na+)的大小关系是___________。
(4)从③组实验结果分析,说明HA的电离程度__________NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是__________。
参考答案:Ⅰ、pH=4
Ⅱ、HA > HC > HB
本题解析:
试题分析:Ⅰ、根据溶液中电荷守恒可知c(H+)=2×2.5×10-4+1.6×10-5+1.4×10-5-4×10-4-2×1.5×10-5=1×10-4,故溶液pH=4;Ⅱ、相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,故酸性HD<HB,NaA溶液呈中性;1mol/L的KC溶液遇酚酞试液呈红色,则HA为强酸,HC为弱酸,同体积、同物质的量浓度的HB、HC分别作导电性试验,发现后者的导电性比前者强,酸性HC>HB,故四种酸的酸性由强到弱的顺序为:HA > HC > HB > HD;Ⅲ、(1)由实验①可知NaA溶液pH=9,故HA为弱酸;(2)①组实验所得混合溶液中由水电离出的c(OH-)= 10-5mol・L-1;(3)②组溶液呈中性故酸过量,则HA的浓度大于0.2 mol/L;混合液中电荷守恒:c(A-)+ c(OH-)=c(Na+)+ c(H+),溶液呈中性:c(OH-)=c(H+),故c(A-)=c(Na+);(4)③组实验溶质为HA与NaA等浓度的混合液,溶液pH<7呈酸性,故HA的电离程度大于A-的水解程度;该混合溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-)。
考点:溶液中离子浓度大小关系。
本题难度:困难
|