微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 50ml0.50mol・L-1盐酸与50mL0.55mol・L-1 NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题
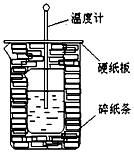
(1)从实验装置上看,图中伤缺少的一种玻璃仪器是________________。
(2)烧杯间填满碎纸条的作用是______________。
(3)若大烧杯上不盖硬纸板,求得的中和热数值___________(填“偏大”“偏小”或“无影响”)。
(4)实验中该用60mL0.50mol・L-1盐酸跟60mL0.55mol・L-1NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热_________(填“相等”或“不相等”),简述理由:____________________________
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会___________;用50mL
0.50mol/LNaOH溶液进行上述实验,测得的中和热数值会_________(填“偏大”“偏小”或“无影响”)。
2、实验题 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题
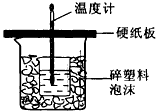
(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3)实验中改用60 mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是_________________________________;所求中和热的数值会________(填“相等”或“不相等”),理由是___________________________。
(4)用相同浓度和体积的氨水(NH3・H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
__________(填“偏大”、“偏小”、“无影响”)。
3、实验题 某实验小组用0.50?mol/L?NaOH溶液和0.50?mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50?mol/L?NaOH溶液
(1)若实验中大约要使用250?mL?NaOH溶液,至少需要称量NaOH固体__________g。
(2)从下图中选择称量NaOH固体所需要的仪器是(填字母):__________。

Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。

(3)某同学进行该实验时未找到环形玻璃棒,实验中他用铜丝代替环形玻璃棒进行搅拌,请说明此做法的缺点:___________________
(4)写出该反应的热化学方程式(中和热为57.3kJ・mol-1)_______________________
(5)取50?mL?NaOH溶液和30?mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:

②近似认为0.50?mol/L?NaOH溶液和0.50?mol/L硫酸溶液的密度都是1?g/cm3,中和后生成溶液的比热容C=4.18J/(g・℃)。则中和热ΔH=__________(取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)__________。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
4、选择题 图所示的实验装置或操作不能达到实验目的是( )
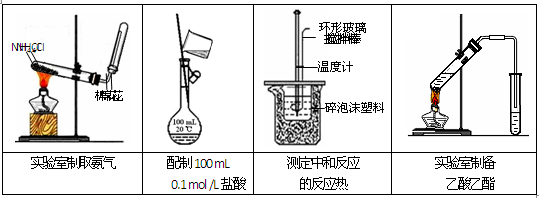
A.①
B.②
C.③
D.④
5、实验题 在下图所示的装置中进行中和反应的反应热测定,实验操作如下
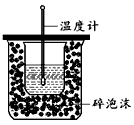
① 用量筒量取50 mL 0.50 mol・L-1盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。
② 把温度计上的酸用水冲洗干净。
③ 用另一个量筒量取50 mL 0.55 mol・L-1 NaOH溶液,并用温度计测量NaOH 溶液的温度,记入下表。
④ 把量筒中的NaOH溶液一次倒入盛有盐酸的小烧杯,轻轻搅拌,并准确读取混合溶液的最高温度,记为终止温度,记入下表。
⑤ 重复实验两次。
(1)实验数据处理(计算平均值)
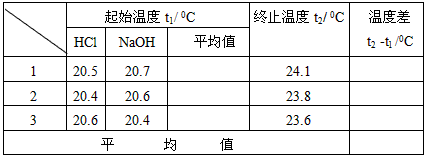
(2)计算反应热:为计算简便,视NaOH溶液和盐酸的密度和比热容与水相同,并忽略实验装置的比热容,近似认为上述NaOH溶液和盐酸溶液的质量各为50g;中和后溶液的比热容c = 4.18 J/(g・°C) 计算生成1mol水时的反应热△H =_______kJ・mol-1
(3)有关实验装置及实验操作方面的问题讨论:
①该实验装置缺少仪器名称是___________,用改正的装置进行实验并回答以下问题。
②如果改用60 mL 0.50 mol・L-1盐酸与60 mL 0.55 mol・L-1NaOH溶液进行反应,与上述实验相比,计算生成1mol水放出的热________(填“偏大”“相等”“偏小”)。
③用相同浓度和体积的醋酸代替盐酸溶液进行上述实验,测得生成1mol水所放出的热________(填“偏大”“偏小”“无影响”)。