微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列是除去括号内杂质的有关操作,其中正确的是( )
A.CO2(CO):通O2,点燃
B.CO(CO2):通过NaOH溶液
C.KNO3(Ba(NO3)2)加入过量K2CO3过滤后向滤液中补加适量HNO3
D.CaO(CaCO3):加水,再过滤
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列有关说法正确的是( )
A.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
B.澄清石灰水能够鉴别二氧化碳和二氧化硫
C.除去FeCl2溶液中的少量FeCl3,可行的办法是加入足量的铜粉
D.金属镁着火时,可以用二氧化碳灭火器来灭火
参考答案:A
本题解析:
本题难度:简单
3、选择题 实验是化学研究的基础.下列关于各实验装置的叙述正确的是( )

A.装置③可用于收集H2、CO2、Cl2、NH3等气体
B.装置②可用于吸收NH3或HCl气体,并防止倒吸
C.装置①常用于分离互不相溶的液体混合物
D.装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
参考答案:A、H2、CO2、Cl2、NH 3等气体和氧气不反应,所以可以
本题解析:
本题难度:简单
4、填空题 某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS),共同生产MnO2和Zn(干电池原料)。
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
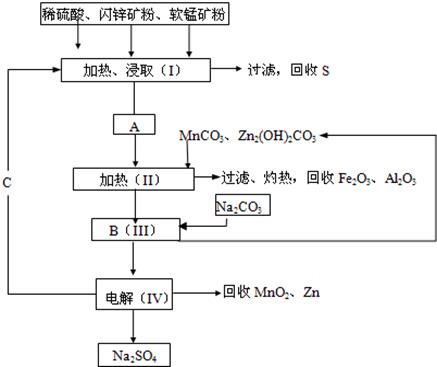
②IV中的电解反应式为MnSO4+ZnSO4+2H2O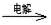 MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。
(1)A中属于还原产物的是?????????。
(2)MnCO3、Zn2(OH)2CO3的作用是?????;Ⅱ需要加热的原因是?????;C的化学式是?????。
(3)Ⅲ中发生的离子方程式为????????,?????????;
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是???????。
参考答案:(1)MnSO4
(2)增大溶液的pH,使Fe3+和A
本题解析:(1)由已知信息条件知,Mn元素化合价由+4价降低为+2价,民以A中还原产物为MnSO4;
(2)由工艺流程图知,MnCO3、Zn(OH)2CO3的作用就是调节pH,使Fe3+和Al3+均生成沉淀。Fe3+、Al3+沉淀容易形成胶体,不利于氢氧化铝、氢氧化铁沉淀,所以Ⅱ加热的目的是加速沉淀生成,防止胶体出现,并使形成胶体的氢氧化铝和氢氧化铁也生成沉淀;操作Ⅰ加热、浸取需要硫酸,由②可知C为硫酸,循环利用。
(4)溶液B中含有Mn2+、Zn2+,根据流程图,加入Na2CO3后,生成MnCO3和Zn2(OH)2CO3,离子方程式是,Mn2++CO32-=MnCO3,2Zn2++2CO32-+H2O=Zn2(OH)2CO3↓+CO2↑。
本题难度:一般
5、选择题 下图中所示的实验方法、装置或操作完全正确的是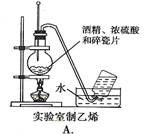
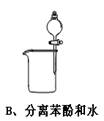

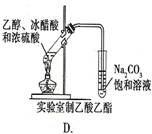
参考答案:B
本题解析:
正确答案:B
A、温度计水银球应在液面以下;B、正确;C、温度计水银球应在蒸馏烧瓶的支管口处;D、右侧的导管应在Na2CO3溶液的液面以上。
本题难度:一般