微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设NA代表阿伏加德罗常数,下列说法正确的是(????)
A.标准状况下,22.4 L氦气和1 mol氟气所含原子数均为2 NA
B.1 mol Na2O2与CO2反应电子转移为2 NA
C.1 mol H2O、1 mol NH3和1mo l OH-所含电子数均为10 NA
D.标准状况下22.4L的氯气和某些物质反应,电子转移一定为2 NA
参考答案:C
本题解析:A、稀有气体为单原子分子,B、过氧化钠中氧为-1价,该反应为歧化反应,转移NA个电子,D、Cl2如发生歧化反应,如与水、氢氧化钠反应,只转移NA个电子。
本题难度:一般
2、选择题 实验室需要用480mL 0.1mol・L-1的硫酸铜溶液,以下配制方法正确的是
[???? ]
A.称取12.5g胆矾(CuSO4・5H2O),配成500mL溶液,待用
B.称取12.5g胆矾(CuSO4・5H2O),加入500mL水,待用
C.称取7.68g无水硫酸铜粉末,加入480mL水
D.称取8.0g无水硫酸铜粉末,加入500mL水,待用
参考答案:D
本题解析:
本题难度:简单
3、填空题 (8分)在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸, 所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示。
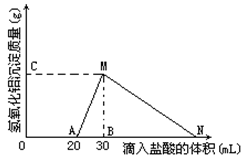
问:
(1)此溶液中同时含有____mol___???离子;
(2)用离子方程式表示MN段发生的反应是????????????
(3)C(或M)点的纵坐标为0.78,则c(AlO2-)=???????????
(4)点B的横坐标为30,则到点N处滴入的HCl溶液体积为???????????????mL
参考答案:(1)0.02mol;OH-?????? (2)Al(OH)
本题解析:
试题分析::(1)由图可知,滴加盐酸开始不产生沉淀,故溶液中还含有OH-,开始加入的20mL盐酸用于中和OH-,由于H++OH-=H2O,故溶液中n(OH-)=n(H+)=0.02L×1mol/L=0.02mol,
故答案为:0.02;OH-;
(2)由图可知,MN段是氢氧化铝与盐酸反应生成氯化铝与水,反应离子方程式为Al(OH)3+3H+=Al3++3H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;
(3)由图可知,从20mL~40mL发生的反应为AlO2
本题难度:一般
4、简答题 (1)0.5molCH4的质量是______,在标准状况下的体积为______;含______个氢原子.
(2)将标准状况下22.4L的HCl溶于水配成200mL的溶液,所得溶液的物质的量浓度为______;
(3)配制300mL0.5mol?L-1氯化钠溶液,需要1.5mol?L-1的氯化钠溶液的体积是______mL.
参考答案:(1)0.5mol甲烷的质量=0.5mol×16g/mol=
本题解析:
本题难度:一般
5、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下,11.2 L CH3OH中含有C-H键1.5NA
B.9g18 8O2中含有的中子数为5NA
C.1 L pH=1的硫酸溶液中含有的H+数为0.2NA
D.1 mol Cu与足量S完全反应生成Cu2S,转移电子数为2NA
参考答案:B
本题解析:
试题分析:甲醇是液体,液体摩尔体积不是22.4L/mol,其物质的量不等于0.5mol,所含碳氢键不等于1.5mol,故A错误;由于n=m/M,则n(18? 8O2)=9g÷36g?molˉ1=1/4mol,1个18? 8O2分子含有(18―8)×2=20个中子,则1/4mol18? 8O2中含有5mol中子,故B正确;pH=1,c(H+)=0.1mol/L,由于n= c?V,则n(H+)=0.1mol/L×1L=0.1mol,故C错误;铜与硫反应生成硫化亚铜,铜元素由0升为+1价,则2Cu+S<
本题难度:一般