��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �����ܡ���Ϊ�������ڵڢ���Ԫ�أ����ǵ����ʷdz����ƣ�Ҳ��Ϊ��ϵԪ�ء�
��1�������ܡ������Ǻܺõ���λ�������γ��塣
��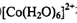 �ڹ�����ˮ����ת��Ϊ
�ڹ�����ˮ����ת��Ϊ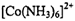 ��д��
��д��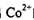 �ļ۲�����Ų�ͼ____��
�ļ۲�����Ų�ͼ____��
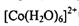 ?��
?��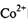 ����λ��Ϊ____��NH3���ӵ�����ԭ���ӻ���ʽΪ____��
����λ��Ϊ____��NH3���ӵ�����ԭ���ӻ���ʽΪ____��
H2O���ӵ����幹��Ϊ__________��
������������һ����̼�����γ��ʻ������磺 �ȡ�CO��N2���ڵȵ����壬��CO������
�ȡ�CO��N2���ڵȵ����壬��CO������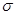 ����
���� ����Ŀ��Ϊ____��д����CO��Ϊ�ȵ������һ�������ӵ����ӷ���____��
����Ŀ��Ϊ____��д����CO��Ϊ�ȵ������һ�������ӵ����ӷ���____��
��2��+2�ۺ�+3����Fe��Co��Ni��Ԫ�س������ϼۡ�NiO��FeO�ľ���ṹ���;����Ȼ��Ƶ���ͬ��Ni2����Fe2�������Ӱ뾶�ֱ�Ϊ69 pm��78 pm�����۵�NiO____FeO��ѡ�<����>����=������ ij����ȻNio���������ͼ��ʾȱ�ݣ�һ��Niz+��ȱ����������Ni2��������Ni3����ȡ�������������Գ������ԡ�ij��������Ʒ���Ϊ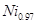 O���þ�����Ni3����Ni2����������֮��Ϊ____��
O���þ�����Ni3����Ni2����������֮��Ϊ____��

�ο��𰸣���1���� ���������
���������
�����������1���������ܡ�������Ԫ�ص�����㶼���������ӣ��������d���ӷֱ�Ϊ6��7��8�����Ը��ݷ��ӵĿռ乹�ͻ�������ж�����ԭ�ӹ�����ӻ���ʽ��sp�� ֱ���� 180��? sp2�� ƽ�������� 120��? sp3�� �������� 109��5���ԭ�ӵ������ﵽ8����ʱ�DZȽ��ȶ��ģ�����CO��˵��̼ԭ���������4�����ӣ���ԭ���������6�����ӣ�Ҫ�γ��ȶ��Ľṹ��̼�����������Ե��ӣ���ԭ�����ṩһ�Ե�����Ϊ��λ��������˫�����ﵽ��8���ӵ��ȶ��ṹ����CO����һ���Ҽ������м���2�����Ӱ뾶ԽС���۵�Խ��
�����Ѷȣ�һ��
2��ѡ���� �������ʺ������Ӽ����ǣ�������
A��Cl2
B��NaOH
C��CO2
D��H2O
�ο��𰸣�B
���������
�����Ѷȣ���
3������� �����֣�����ѧ-���ʽṹ�����ʡ�
̼��Ԫ�ذ�����C��Si�� Ge�� Sn��Pb��
(1)̼�����е������ʯī��������ɣ���ṹ������ʯī���壬ÿ��̼ԭ��ͨ�����������ӻ�����Χ̼ԭ�ӳɼ������̼���ܵIJ����֮�俿�������������һ��
(2)CH4�й��õ��Ӷ�ƫ��C��SiH4�й��õ��Ӷ�ƫ��H����C��Si��H�ĵ縺���ɴ�С��˳�� Ϊ����������
����������
(3)�ü۲���ӶԻ��������ƶ�SnBr2������Sn��Br�ļ���������120�㣨�������������������
(4)Ǧ���������γɵ�ij������ľ����ṹ�ǣ�Pb 4+���������������㣬Ba2+���ھ������ģ�O2-���ھ���������ģ��û����ﻯѧʽΪ��������
4+���������������㣬Ba2+���ھ������ģ�O2-���ھ���������ģ��û����ﻯѧʽΪ�������� ��������ÿ��Ba2+������������O2-��λ��
��������ÿ��Ba2+������������O2-��λ��
�ο��𰸣�
(1) sp2???���»���
(2) C��H
�����������
�����Ѷȣ���
4��ѡ���� ���ʵ��������ʲ����ü��������͵���(����)
A�������Ļ�ѧ����û����������
B��HF��HCl�ȶ�
C�����ʯ���۵�Ⱦ�����
D�����������Һ̬����ʹ�̬
�ο��𰸣�D
���������
��������������л������������ܴ������ȶ���A�ͼ����й�ϵ�����ӵ��ȶ��Ժ��ۼ�ǿ���й�ϵ��B�ͼ����йأ�C�ж���ԭ�Ӿ��壬�۵�ͼ��ܴ�С�й�ϵ��D���γɵ��Ƿ��Ӿ��壬�۷е�ͷ��Ӽ��������й�ϵ���ͼ����أ���ѡD��
��������������̬��̬ԭ���γ�1mol��ѧ��ʱ�ͷŵ�������������ڼ������ķ��룬��֮�����������ǻ�ѧ���������ڼ��ܡ�
�����Ѷȣ�һ��
5������� ����ѧ����ѡ��3�����ʽṹ�����ʡ���15�֣�
��֪X��Y��Z����Ԫ�ص�ԭ������֮�͵���48��X��һ��1��2���⻯������м��ЦҼ����Цм�������ԭ�ӹ�ƽ�档Z�ǽ���Ԫ�أ�Z�ĵ��ʺͻ������й㷺����;����֪Z�ĺ˵����С��28���Ҵ������2��δ�ɶԵ��ӡ���ҵ������ZO2��̼�ᱵ������״̬����ȡ������M��M�ɿ���һ�ֺ������Σ�����X���߷�����M�������С�ظ���ԪΪ�����壨����ͼ��������λ��ΪZ4+��ռ������λ��ΪBa2+��ռ����������λ��ΪO2�C��ռ��
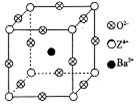
��1��Y2+�Ľṹʾ��ͼ________________��Z�ļ۲�����Ų�ʽΪ____________��
��2��X�ڸ��⻯������_____________��ʽ�ӻ���X��Y�γɵĻ�����YX2�ĵ���ʽΪ_____________________��
��3�����Ʊ�M�Ļ�ѧ��Ӧ����ʽ��______________________________________��
����M�����У�����Z4+��������������ģ�Ba2+����������Ķ��㣬��O2�C�����������_______________��
����֪O2�C�뾶Ϊ1.4��10�C10 m��Z4+�İ뾶Ϊ6.15��10�C11m������ӵ�����ΪNA����M���ܶ�Ϊ_______________g��cm�C3�������ػ���
�ο��𰸣�����(3)��3��,����ÿ��2��,��15�֣�
��1��
���������
��X��һ��1��2���⻯������м��ЦҼ����Цм�������ԭ�ӹ�ƽ�档��XΪ̼������Z�ǽ���Ԫ�أ�Z�ĵ��ʺͻ������й㷺����;����֪Z�ĺ˵����С��28���Ҵ������2��δ�ɶԵ��ӡ�ZΪ22���ѣ�1s22s22p63d24s2��YΪ48-6-22=20���ơ�
��1��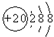 ?? 3d24s2???????????
?? 3d24s2???????????
�����Ѷȣ�һ��