微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质性质的变化规律,与共价键的键能大小有关的是[???? ]
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI的热稳定性依次减弱
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.NaF、NaCl、NaBr、NaI的熔点依次降低
参考答案:BC
本题解析:
本题难度:一般
2、选择题 在化学上,常用一条短线表示一个化学键,如图所示的有关结构中,有直线(包括虚线)不表示化学键或分子间作用力的是[???? ]
A.石墨的结构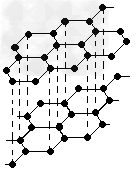
B.P4的结构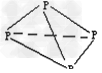
C.CCl4的结构
D.立方烷的结构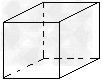
参考答案:C
本题解析:
本题难度:简单
3、选择题 关于氢键,下列说法正确的是
A.每一个水分子内含有两个氢键
B.冰和水中都存在氢键
C.DNA双螺旋的两个螺旋链不是通过氢键相互结合的
D.H2O是一种非常稳定的化合物,这是由于氢键所致
参考答案:B
本题解析:
试题分析:水分子内不存在氢键,A不正确;DNA双螺旋的两个螺旋链是通过氢键相互结合的,C不正确;水分子的稳定性和化学键有关系,与氢键无关,D不正确,答案选B。
点评:该题是基础性试题的考查,也是高考中的常见考点之一。试题主要是考查学生对氢键概念的了解掌握程度,以及灵活运用氢键解决实际问题的能力,难度不大。该题有利于培养学生的逻辑思维能力和发散思维能力。
本题难度:一般
4、填空题 CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:
①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
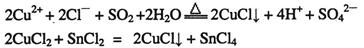
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子: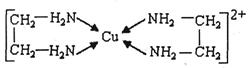 ???
???
请回答下列问题:
(1)基态Cu原子的核外电子排布式为????????????????,H、N、O三种元素的电负性由大到小的顺序是????????????。
(2)SO2分子的空间构型为????????,与SnCl4互为等电子体的一种离子的化学式为????????????。
(3)乙二胺分子中氮原子轨道的杂化类型为????????????,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是???????????????????????????。
(4)②中所形成的配离子中含有的化学键类型有??????????。(填字母)
A?配位键???? B?极性键???? C?离子键??? D?非极性键
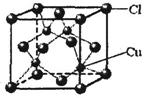
(5)CuCl的晶胞结构如上图所示,其中Cl原子的配位数为??????????。
参考答案:
(1)1s22s22p63s23p63d104s1或
本题解析:略
本题难度:简单
5、填空题 下表是元素周期表的一部分.
| 周期族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA
1
①
2
②
③
④
⑤
⑥
3
⑦
⑧
⑨
⑩
(1)元素①~⑩中原子半径最大是______(填元素符号),它的原子结构示意图为______.
(2)元素④氢化物的分子结构呈______型,它是由______键形成的______分子(后两空填“极性”或“非极性”).
(3)⑨的单质是良好的半导体材料,工业上常用④的单质与⑨的氧化物来制备粗制的⑨的单质,请写出该反应的化学方程式______.
(4)请写出元素⑦、⑧的最高价氧化物的水化物之间反应的离子方程式:______.
参考答案:由元素在周期表的位置可知,①为H,②为Li,③为Be,④为C
本题解析:
本题难度:一般
|