微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在含有Mg2+、Fe2+、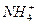 、Al3+的溶液中,加入过量的氢氧化钠水溶液,加热搅拌,再加入过量盐酸,溶液中减少的阳离子是
、Al3+的溶液中,加入过量的氢氧化钠水溶液,加热搅拌,再加入过量盐酸,溶液中减少的阳离子是
A.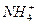
B.Fe2+
C.Mg2+
D.Al3+
参考答案:AB
本题解析:Mg2+、Al3+经转化后总量不变,Fe2+转化为Fe3+,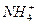 ?部分转化为NH3(挥发),均减少。
?部分转化为NH3(挥发),均减少。
本题难度:简单
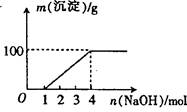
2、选择题 某澄清透明溶液中只可能含有①Al3+;② Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32+;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示。则该溶液中一定含有的离子是:(??)
A.②⑤⑥⑦
B.②③⑤⑦
C.①②③⑥⑦
D.①②③④⑤⑦
参考答案:B
本题解析:
试题分析:向该溶液中加入NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子,在酸性溶液中CO32-离子与H+离子反应生成CO2气体而不能存在,根据溶液的电中性可知一定含有阴离子,则一定含有NO3-离子;而后才有沉淀,能够生成沉淀的是Fe3+、Fe2+或Al3+或Mg2+中的一种或几种,但在酸性条件下Fe2+离子与NO3-离子发生氧化还原反应而不能共存,则一定不含Fe2+离子,沉淀达最大量后继续滴加NaOH溶液沉淀不减少消失.说明一定不含有Al3+;在NaOH溶液为4mol
本题难度:一般
3、选择题 下列各组离子一定能大量共存的是
A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
B.在强碱溶液中:Na+、K+、AlO2-、CO32-
C.在c(H+)=10-13mol/L的溶液中:NH4+、Al3+、SO42-、NO3-
D.在pH=0的溶液中:K+、Fe2+、Cl-、NO3-
参考答案:B
本题解析:分析:A.Fe3+与SCN-发生络合反应;
B.强碱溶液中存在大量的OH-;
C.c(H+)=10-13mol/L的溶液呈碱性,存在大量的OH-;
D.pH=0的溶液呈酸性,存在大量的H+.
解答:A.Fe3+与SCN-发生络合反应生成Fe(SNC)3而不能共存,故A错误;
B.强碱溶液中存在大量的OH-,离子之间不发生任何反应,可以大量共存,故B正确;
C.c(H+)=10-13mol/L的溶液呈碱性,存在大量的OH-,NH4+与OH-反应生成NH3?H2O,A13+与OH-反应生成沉淀而不能大量共存,故C错误;
D.pH=0的溶液呈酸性,存在大量的H+,Fe2+与NO3-发生氧化还原反应而不能大量共存,故D错误.
故选B.
点评:本题考查离子共存问题,题目难度中等,注意常见离子的性质,判断离子之间能否发生反应,注意题目的要求.
本题难度:简单
4、填空题 有一瓶无色溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、I-、Cl-、NO3-、CO32-、SO42-,取该溶液进行以下实验:
(1)该溶液可使pH值试纸呈现红色;
(2)取溶液少量加新制氯水及CCl4振荡,可见CCl4层呈现紫色;
(3)取溶液少量加氯化钡溶液,有白色沉淀生成,加入HNO3后沉淀不溶解;
(4)取实验(3)之上层清液,加入硝酸银溶液有白色沉淀生成,加入HNO3后沉淀不溶解;
(5)取原溶液少量加入NaOH溶液呈碱性,在此过程中有白色沉淀生成,而后又逐渐消失,将此溶液加热,有无色气体放出,该气体能使润湿的红色石蕊试纸变蓝。
(1)根据上述实验事实,溶液中肯定存在的离子有____________________
(2)肯定不存在的离子有__________________?????????????_,
(3)不能确定是否存在的离子有___________??????????。
参考答案:(1)NH4+、Al3+、I-、SO42-(2)Mg2+、B
本题解析:溶液是无色的,所以一定没有Fe3+;根据(1)可知溶液显酸性,则CO32-一定没有;根据(2)可知生成物是单质碘,因此一定含有I-,所以就没有NO3-;根据(3)可知白色沉淀是硫酸钡,则一定含有SO42-,所以一定没有Ba2+;实验(4)中白色沉淀是氯化银,但由于加入了氯水,所以无法确定是否含有氯离子;根据(5)可知白色沉淀是氢氧化铝,气体是氨气,所以NH4+、Al3+一定含有,但Mg2+不存在;其中钾离子无法确定。
本题难度:一般
5、选择题 下列说法正确的是
A.90℃时,纯水的pH等于7
B.已知一种c (H+)=1×10-3mol/L的酸和一种c (OH-)=1×10-3mol/L碱溶液以等体积混合后,溶液呈酸性,其原因是浓的弱酸和稀碱反应所致
C.配制FeCl3溶液,为了抑制水解,常加稀硫酸
D.在Na2S溶液中,离子浓度的关系是:c (Na+)>c (S2-)>c (HS-)>c (OH-)>c (H+)
参考答案:B
本题解析:A错,90℃时,纯水的pH小于7;B正确,若溶液呈酸性则该酸为越酸所致;C错,配制FeCl3溶液,为了抑制水解,常加稀盐酸;D错,离子浓度的关系是:c (Na+)>c (S2-)>c (OH-)>c (HS-)>c (H+)
本题难度:一般