微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 
(7分)某无色溶液,其中可能存在Na+、Ba2+、AlO2-、SO32-、SO42-,取该溶液进行有关实验,实验结果如图所示:试回答下列问题:
(1)气体甲的化学式为????????????????。
(2)由溶液甲生成沉淀乙的离子方程式为???????????????????????????。
(3)沉淀丙中一定含有??????????????,可能含有?????????????????。
(4)综合上述信息,该溶液中肯定存在的离子有?????????????????????。
参考答案:(1) SO2 (2)Al3++3HCO3-![]()
本题解析:略
本题难度:一般
2、选择题 向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中各离子数目也相应地发生变化。溶液中各离子数目与图中四条曲线的对应关系完全正确的是
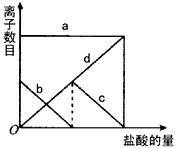
[???? ]
a?
b
?c
d
A.
Cl-
K+
CO32-
HCO3-
B.
K+?
CO32-
Cl-
HCO3-
C.
K+?
CO32-
HCO3-
Cl-
D.
K+?
HCO3-
Cl-
CO32-
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列各组离子中可能在某无色溶液中大量共存的是
A.MnO4-、K+、Na+、SO42-
B.K+,H+,CO32-,Cl-
C.Mg2+、NH4+、Cl-、NO3-
D.Ba2+、K+、HCO3-、OH-
参考答案:C
本题解析:
本题难度:简单
4、选择题 某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A.Na+
B.CO32-、NH4+
C.CH3COO-
D.CH3COO-、Na+
参考答案:C
本题解析:试题分析:某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,首先Na2O2先和水反应生成氢氧化钠和氧气,钠离子变大,HCO3-与氢氧根反应生成CO32-,所以HCO3-变小、CO32-变大,故选C。
考点:离子反应,过氧化钠的性质。
点评:离子反应,离子共存的变形形式,抓住题眼,找到突破口。
本题难度:困难
5、选择题 常温下,下列有关溶液中微粒的物质的量浓度关系正确的是
A.pH均为9的①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液,其物质的量浓度的大小顺序为:①>②>③
B.向饱和氯水中加入NaOH溶液至pH=7,所得溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-)
C.0.1 mol・L-1 KHC2O4溶液中:c(OH-)=c(H+) +c(H2C2O4)-2c(C2O42-)
D.等物质的量浓度Na2CO3溶液和NaHCO3溶液等体积混合,所得溶液中:c(CO32-)+c(OH-)< c(H+)+c(HCO3-)+3c(H2CO3)
参考答案:D
本题解析:试题分析: A、酸性CH3COOH>H2CO3>HCO3-,所以同浓度溶液的碱性:CH3COONa<Na2CO3,pH均为9的三溶液,物质的量浓度CH3COONa最大、NaOH最小,错误;B、饱和氯水中加入氢氧化钠溶液至中性,c(ClO-)<c(Cl-),错误;C、KHC2O4溶液电荷守恒式为c(K+)+c(H+)=2c(C2O42-)+c(HC2O4-)+c(OH-)、物料守恒式为c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),所以c(OH-)=c(H+) +c(H2C2O4)-c(C2O42-),错误。D、等浓度、等体积碳酸钠与碳酸氢钠溶液混合,电荷守恒式为c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)、物料守恒式为2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)],消去c(Na+)得:2c(OH-)+c(CO32-)=c(HCO3-)+3c(H2CO3)+2c(H+),因溶液呈碱性,c(OH-)>c(H+),所以c(CO32-)+c(OH-)< c(H+)+c(HCO3-)+3c(H2CO3),正确。
考点: 离子浓度比较
本题难度:一般