��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���б仯�У����ڷֽⷴӦ��������������ԭ��Ӧ����[???? ]
A������̼�����
B������������ȷֽ�
C������ʯ��ʯ
D����һ����̼����ͨ�����ȵ�����ͭ��ĩ
�ο��𰸣�B
���������
���������
���б仯�У����ڷֽⷴӦ��������������ԭ��Ӧ����A������̼����泥��ǷֽⷴӦ��������������ԭ��Ӧ����Ӧǰ�ϼ۲��䣬����
B������������ȷֽ⣬�ǷֽⷴӦ��Ҳ��������ԭ��Ӧ����Ӧǰ����Ԫ�ػ��ϼ۵ı仯����ȷ��
C������ʯ��ʯ���ǷֽⷴӦ��������������ԭ��Ӧ����Ӧǰ�ϼ۲��䣬����
D����һ����̼����ͨ�����ȵ�����ͭ��ĩ�����ǷֽⷴӦ������������ԭ��Ӧ����Ӧǰ�ϼ۱仯������
�����Ѷȣ���
2������� �������ƣ�NaH2PO2�������ڻ�ѧ��������ͨ����ѧ��Ӧ�����϶Ƽ�������������Ͻ�
��1����ѧ��������Һ�к���Ni2+��H2PO2���������������·������¶�����Ӧ��
��????Ni2+ + ?????H2PO2��+ ??????�� ???Ni?+??????H2PO3��+ ????
�� 6H2PO2- +2H+ ��2P+4H2PO3-+3H2��
����ƽ��Ӧʽ�١�
��2����Ӧʽ���л�ԭ����???????������ԭԪ����????????��
��3����Ӧ���У�������1 mol H2PO3-����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ??????????��
��4���Ӷ�����ѧ������Ӧ������������1mol Ni��1mol P��ͬʱ��????mol H2PO3�����ɡ�
��5��������и�С���еĻ�ѧ��Ӧ����ʽ���������O2��Ӧ����������ϸ��ӣ�����ͨ�������K2O�����������K2O2�����г�������ͳ�������ȡ�Ҫ�Ʊ����������ͨ������һ�����ü������ԭ��Ӧ�Ĺ�����������λ��������Ρ�д�����л�ѧ��Ӧʽ��
������������Ʒ�Ӧ???????????????
�ڼػ�ԭ����ػ�������һ�ֵ�������??????????????????
�ο��𰸣���1�� 1��1��1 H2O��1��1��2H+����2�� H2PO
���������
�����������1�����ݻ��ϼ�������ȣ���Ԫ�صĻ��ϼ���+2��ת��Ϊ0�ۣ�������2�ۣ���Ԫ�صĻ��ϼ���+1��ת��Ϊ+3�ۣ����ߵ�2�ۣ��ٸ���ԭ���غ�͵���غ���ƽ����ʽ��Ni2++H2PO2-+H2O�TNi+H2PO3?-+2H+����Ϊ��1��1��1 H2O��1��1��2H+����2����Ӧʽ�٣�H2PO2������Ԫ�صĻ��ϼ���+1��ת��ΪH2PO3���е�+3�ۣ����ϼ����ߣ�����������ԭ������Ԫ�صĻ��ϼ���+2��ת��Ϊ0�ۣ����ϼ۽��ͱ���ԭ����3����4���ɷ�Ӧ��֪������1mol Niͬʱ����1mol H2PO
�����Ѷȣ�һ��
3��ѡ���� ������������������һ�������·�Ӧʱ������������ԭ������
A��������Һ
B��������Һ
C������
D��������
�ο��𰸣�B
���������
��������������������ᷢ��������Ӧ��δ����������ԭ��Ӧ��Aѡ��������⡣��������������Һ��Ӧ�������ǵ�ȩ����������������Һ��Ӧ����ԭ����ʱ����������ԭ����Bѡ��������⡣������������������ԭ��Ӧ����������ԭ����Cѡ��������⡣������������Ʒ�Ӧ������������ԭ����Dѡ��������⡣��ѡB��
�����������Ǿ߱�ȩ������������������Һ��Ӧ����������Ӧ��
�����Ѷȣ���
4��ѡ���� ClO2��һ������ɱ��Ч�ʸߡ�������ȾС��ˮ��������ʵ���ҿ�ͨ�����·�Ӧ�Ƶ�ClO2��2KClO3+H2C2O4+H2SO4 2ClO2��+2CO2��+K2SO4+2H2O������˵����ȷ���� [???? ]
2ClO2��+2CO2��+K2SO4+2H2O������˵����ȷ���� [???? ]
A��KClO3�ڷ�Ӧ�еõ�����
B��ClO2����������
C��H2C2O4�ڷ�Ӧ�б���ԭ
D��1mol KClO3�μӷ�Ӧ����2 mol����ת��
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5������� ��9�֣��������ƣ�NaClO2����һ����Ҫ�ĺ�������������Ҫ����ˮ�������Լ�ɰ�ǵ�Ư����ɱ�����������ù������ⷨ�����������ƵĹ�������ͼ��
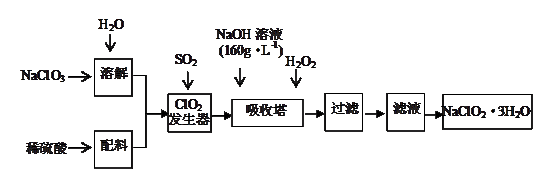
��֪��NaOH��Һ��160g��L-1����ָÿ����Һ�к�����160 g��
�Իش��������⣺
��1����NaOH��Һ�����ʵ���Ũ��Ϊ???????????��
��2�����������У�ClO2��NaOH��H2O2��Ӧ����NaClO2��O2����÷�Ӧ�л�ԭ���������������ʵ���֮��Ϊ?????????��
��3��NaClO2���ȶ�����������ڼ���ʱ���û�ʱ������������ը���䱬ը��IJ��������
?????????������ĸ��
A��NaCl��Cl2
B��NaCl��NaClO
C��NaClO3��NaClO4
D��NaCl��NaClO3
(4)NaClO3��SO2��Ӧ����ClO2��д���÷�Ӧ�Ļ�ѧ����ʽ�����õ����ű������ת�Ƶķ������Ŀ��?????????????????????????????????????????????????????????????????��
�ο��𰸣���1��4mol/L ------2��??��2��1:2----
�����������1��NaOH��Һ��160g��L-1���������ʵ���Ũ����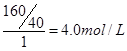 ��
��
��2����Ԫ�صĻ��ϼ۴ӣ�4�۽��͵���3�ۣ���Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0�ۣ�����������ClO2�ͻ�ԭ��H2O2�����ʵ���֮����2�U1��
��3�����������֪����Ԫ�صĻ��ϼۼ����ߣ������ͣ�����ѡ��D��ȷ��
��4����Ԫ�صĻ��ϼ۴ӣ�5�۽�
�����Ѷȣ�һ��