��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ���ܱվ�������(W)�У����������������淴Ӧ����A(g)��2B(g) 3C(g)��D(s)? ��H1>0����xM(g)��N(g)
3C(g)��D(s)? ��H1>0����xM(g)��N(g) 3Q(g)����H2����Ӧ���и������뷴Ӧ���и����ʾ���������Ӧ����ij������ֻ���з�Ӧ�ڣ�M��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
3Q(g)����H2����Ӧ���и������뷴Ӧ���и����ʾ���������Ӧ����ij������ֻ���з�Ӧ�ڣ�M��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
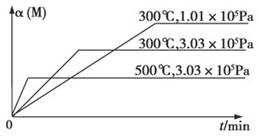
���ж�W�����н��еķ�Ӧ�ƶϺ�������
A����Ӧ��һ�����Է���Ӧ����Ӧ��һ���Ƿ��Է���Ӧ
B�����������¶ȱ��ֲ��䣬��v��(B):v��(C)��2:3
C������ѹ�����£�����N����C�����ʵ�����С
D�������¶ȣ�������Ӧ��ƽ�ⳣ������С
2��ѡ���� һ���¶��µĶ��������У���ӦA2��g��+B2��g�� ?2AB��g���ﵽƽ���־����
?2AB��g���ﵽƽ���־����
A����λʱ��������2n mol ABͬʱ����n mol B2
B����λʱ�������ʵ�������ʱ��ı仯���仯
C����λʱ��������n mol A2ͬʱ����n mol B2
D�������ڸ���ֵ����ʵ�������ʱ��ı仯���仯
3��ѡ���� ����˵����ȷ���ǣ�?��
A?���Է����еķ�Ӧһ�����ܷ������Է����еķ�Ӧһ����Ѹ�ٷ���
B?���ʷ�����ѧ��Ӧ�������������仯�������������仯�����ʱ仯���ǻ�ѧ�仯
C?���Ȼ����ij����ܽ�ƽ����ϵ�У���������ˮ���Ȼ�����Ksp����
D?���Ȼ����ij����ܽ�ƽ����ϵ�У�����⻯�ع��壬�Ȼ���������ת��Ϊ�⻯������
4��ѡ���� ������ʵ��������������ԭ�����͵��ǣ�??��
A������ơ��ƿ��ƿ�����Ϸ��������ĭ������
B���μӷ�̪�İ�ˮ�м����Ȼ�粒�����ɫ��dz
C����H2��I2��g����HI��ɵ�ƽ����ϵ����ѹ����ɫ����
D����ҵ����������Ĺ�����ʹ�ù����Ŀ�������߶��������������
5��ѡ���� ��10�֣���1����֪���淴Ӧ��M(g)��N(g) P(g)��Q(g)?��H��0��
P(g)��Q(g)?��H��0��
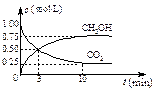
��Ҫ����Q��Ũ�ȣ��������������������¿��Բ�ȡ�Ĵ�ʩΪ????������ţ���
A������һ����M???? B�����ͷ�Ӧ�¶�???? C�����߷�Ӧ�¶�????
D����С�������???? E���������?????? F�������һ����P
��2����˹�����������Ϳ�ѧ�о����к���Ҫ�����塣��Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã�����ͨ����ӵķ����ⶨ���ָ�������3���Ȼ�ѧ��Ӧ����ʽ��
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)???????��H����24.8 kJ��mol��1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)???��H����47.2 kJ��mol��1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g)??????��H����640.5 kJ��mol��1
д��CO���廹ԭFeO����õ�Fe �����CO2������Ȼ�ѧ��Ӧ����ʽ��
_________________???????????????????????????????????????????????????????????��
��3�������Ϊ1 L���ܱ������У�����1 mol CO2��3 mol H2��һ�������·�����Ӧ�� CO2(g)+3H2(g) CH3OH(g)+H2O(g)? ��H=��49.0 kJ/mol�� ��
CH3OH(g)+H2O(g)? ��H=��49.0 kJ/mol�� ��
��CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��
�ٴ�3 min��10 min��v(H2)=?????mol/(L��min)��
����˵��������Ӧ�ﵽƽ��״̬����?????????��ѡ���ţ���
A����Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1�U1����ͼ�н���㣩
B�����������ܶȲ���ʱ��ı仯���仯
C����λʱ����ÿ����3 mol H2��ͬʱ����1 mol H2O
D��CO2����������ڻ�������б��ֲ���
�����д�ʩ����ʹn (CH3OH)/n (CO2)�������????????��ѡ���ţ���
A�������¶�????????????????????? B�����º��ݳ���He(g)
C����H2O(g)����ϵ�з���????????? D�����º����ٳ���1 mol CO2��3 mol H2