微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)
(1)实验室在临时配制一些FeCl2的溶液时,常将氯化亚铁固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,是为了 。稀释后还需要加入一些铁粉,其目的是 ,相关反应的离子方程式为 。
(2)氯化铁水溶液呈 性,原因是(用离子方程式表示):___________ ____ 。 把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。如果要从氯化铁溶液得到纯氯化铁固体,常采用的方法是 。
参考答案:(12分)(1)抑(防)止Fe2+水解(2分); 防止Fe2+被氧化成Fe3+(2分) ;
2Fe3+ + Fe = 3Fe2+ (2分)
(2)酸性(1分); Fe3+ + 3H2O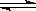 Fe(OH)3 + 3H+(2分,写“=”不得分)
Fe(OH)3 + 3H+(2分,写“=”不得分)
氧化铁或Fe2O3(1分); 将三氯化铁溶液在HCl环境(或气氛)中加热蒸干(2分)
本题解析:(1)Fe2+离子会发生水解,离子方程式为: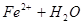 ?
?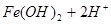 ,用浓盐酸溶解是为了抑(防)止Fe2+水解;又由于Fe2+离子易被氧气氧化生成
,用浓盐酸溶解是为了抑(防)止Fe2+水解;又由于Fe2+离子易被氧气氧化生成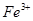 ,所以加入铁粉是为了防止Fe2+被氧化成Fe3+:
,所以加入铁粉是为了防止Fe2+被氧化成Fe3+: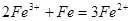 ;
;
(2)氯化铁水溶液呈酸性,原因是:Fe3+ + 3H2O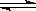 Fe(OH)3 + 3H+;把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是:Fe2O3;要从氯化铁溶液得到纯氯化铁固体,应将三氯化铁溶液在HCl环境(或气氛)中加热蒸干;
Fe(OH)3 + 3H+;把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是:Fe2O3;要从氯化铁溶液得到纯氯化铁固体,应将三氯化铁溶液在HCl环境(或气氛)中加热蒸干;
本题难度:简单
2、填空题 (6分)(1)有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC用同样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为 。
(2)NO2可用氨水吸收生产硝酸铵,25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是 (用离子方程式表示)。向该溶液中滴加bL氨水后溶液显中性,则滴加氨水的过程中水的电离平衡将会 (填“正向”、“逆向”或“不”) 移动,所滴加氨水的浓度为 mol/L。(已知氨水的电离平衡常数Kb=2×10-5)
参考答案:(6分) (1) HA、HC、HB、HD (2)NH4++H2O NH3・H2O+H+ ,逆向 ,
NH3・H2O+H+ ,逆向 ,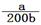
本题解析:(1)相同物质的量浓度的NaD和NaB溶液的pH,前者比后大,NaA溶液呈中性,根据越弱越水解,水解后碱性越强可知HB比HD强,但二者都是弱酸,HA的盐不会水解证明是强酸;lmol/l的KC溶液遇酚酞试液呈红色,HC的盐会水解显碱性证明是弱酸;同体积,同物质的量浓度的HB,HC用的装置分别做导电性试验,发现后者的灯泡比前者亮,说明HC的电离程度大于HB的电离程度,HC强于HB,综上所述:HA>HC>HB> HD;
(2)硝酸铵溶液呈酸性原因是NH4+离子水解:NH4+ + H2O  NH3・H2O + H+,水中存在H2O
NH3・H2O + H+,水中存在H2O  H+ + OH-,当加入铵根离子后,铵根离子与OH-结合形成氨水分子NH4++ OH-
H+ + OH-,当加入铵根离子后,铵根离子与OH-结合形成氨水分子NH4++ OH- NH3・H2O,消耗的OH-由水分子继续电离提供,因此铵根水解的过程实际上是水分子电离增大的过程,然后向溶液中滴加氨水,由于氨水电离提供的OH-要远大于水电离提供的OH-,这样滴加氨水后,水分子的电离程度是减小的,选“逆向”; 根据氨水电离方程NH3・H2O
NH3・H2O,消耗的OH-由水分子继续电离提供,因此铵根水解的过程实际上是水分子电离增大的过程,然后向溶液中滴加氨水,由于氨水电离提供的OH-要远大于水电离提供的OH-,这样滴加氨水后,水分子的电离程度是减小的,选“逆向”; 根据氨水电离方程NH3・H2O  NH4+ + OH-,[OH-]=(Kb×[NH3?H2O])/[NH4+],由于溶液体积不管最终是多少,NH4+与NH3?H2O浓度比与其物质的量之比相同,即[OH-]=Kb×n(NH3?H2O)/n(NH4+) , 10-7=2×10-5n(NH3?H2O)/a, 解得 n(NH3?H2O)=a/200,所滴加氨水的浓度为
NH4+ + OH-,[OH-]=(Kb×[NH3?H2O])/[NH4+],由于溶液体积不管最终是多少,NH4+与NH3?H2O浓度比与其物质的量之比相同,即[OH-]=Kb×n(NH3?H2O)/n(NH4+) , 10-7=2×10-5n(NH3?H2O)/a, 解得 n(NH3?H2O)=a/200,所滴加氨水的浓度为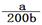 mol/L。
mol/L。
考点:考查弱电解质的电离,盐的水解等知识。
本题难度:困难
3、填空题 (16分)常温下,将某可溶性一元碱XOH和HCl溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
实验编号
| XOH物质的量浓度(mol・L-1)
| HCl物质的量浓度(mol・L-1)
| 混合溶液的pH
|
甲
| 0.2
| 0.2
| pH=a
|
乙
| c
| 0.2
| pH=7
|
丙
| 0.2
| 0.1
| pH<7
|
丁
| 0.1
| 0.1
| pH=5
|
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明XOH是强碱还是弱碱_________________________________________________________。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。混合液中离子浓度c(Cl-)与 c(X+)的大小关系是________________________。
(3)丙组实验结果分析,XOH是________碱(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是________________________________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol・L-1。写出该混合溶液中下列算式的精确结果(不能做近似计算)。
c(Cl-)-c(X+)=________mol・L-1 c(H+)-c(XOH)=________mol・L-1
参考答案:(1)若a=7,则XOH是强碱;若a<7,则XOH是弱碱 ; (2)否;c(Cl-)=c(X+)
(3)弱 ;c(Cl-) >c(X+)> c(H+) > c(OH-) ;(4)10-5 10-5-10-9 10-9
本题解析: (1)由于盐酸是一元强酸,若XOH是一元强碱,则等体积混合时溶液的pH=7;若XOH是一元弱碱,则等体积混合时溶液的pH<7;(2)由于不能确定XOH的强弱,所以不考虑其它组的实验结果,单从乙组情况分析,C不一定等于0.2;由于pH=7,则c(H+)=c(OH-);在溶液中存在电荷守恒,即c(Cl-) + c(OH-) = c(H+)+c(X+),盐酸混合液中离子浓度c(Cl-)与 c(X+)的大小关系是c(Cl-)=c(X+);(3)由于碱的浓度大于酸的浓度而二者的体积相等,溶液的pH<7,说明碱是弱碱;由于溶液显酸性,所以c(H+) > c(OH-);根据溶液的电荷守恒可知:c(Cl-) >c(X+),盐的电离远大于水的电离作用,所以c(X+)> c(H+),故该混合溶液中离子浓度由大到小的顺序是c(Cl-) >c(X+)> c(H+) > c(OH-);(4)二者恰好完全反应生成正盐。盐水解消耗水电离产生的OH-,所以溶液显酸性,水电离产生的H+和OH-的浓度相等,所以丁组实验所得混合溶液中由水电离出的c(OH-)=10-5mol/L;因为c(Cl-) + c(OH-) = c(H+) +c(X+),所以c(Cl-)-c(X+)=c(H+)-c(OH-) = (10-5-10-9)mol/L;根据质子守恒可知c(H+)= c(OH-)+c(XOH),所以c(H+)-c(XOH)=c(OH-)=10-9mol/L。
考点:考查电解质强弱的判断、离子浓度的大小比较、盐的水解的知识。
本题难度:一般
4、填空题 (12分)(1)25℃时,pH=12.0的KOH溶液中,由水电离出的c(OH-)=_______mol/L;pH=12.0的K2CO3溶液中,由水电离出来的c(OH-)=_______mol/L。
(2)常温下0.1mol・L-1 CH3COONa溶液PH=8
①用离子方程式表示CH3COONa溶液PH=8的原因: 。
②按物质的量浓度由大到小顺序排列该溶液中各种微粒(水分子除外) 。
(3)FeCl3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): 。
参考答案:(1)1×10-12 1×10-2 (2) CH3COO- + H2O CH3COOH + OH-
CH3COOH + OH-
c(Na+)>c(CH3COO-)>c(OH-)>c(H+) (3)酸性 Fe3++3H2O  Fe(OH)3+3H+
Fe(OH)3+3H+
本题解析:(1)酸、碱抑制水电离,含有弱根离子的盐促进水电离,碱溶液中水电离出的c(OH-)=c(H+)=10-12 mol/L,K2CO3是强碱弱酸盐,促进水电离,溶液中水电离出的c(OH-) 为水的离子积常数与c(H+)的比,所以水电离出来的c(OH-)=10?14/10?12mol/L=10-2 mol/L。
(2)①醋酸钠中醋酸根离子能水解,导致溶液显示碱性,即CH3COO-+H2O CH3COOH +OH-,
CH3COOH +OH-,
②在CH3COONa 溶液中,CH3COO-因水解而减少,该溶液因水解显碱性,则按物质的量浓度由大到小顺序排列该溶液中各种微粒为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
(3)FeCl3的水溶液中,由于Fe3+的水解,导致溶液呈酸性,离子方程式为Fe3++3H2O  Fe(OH)3+3H+ .
Fe(OH)3+3H+ .
考点:考查影响水电离平衡的因素,盐类水解的应用等知识。
本题难度:一般
5、选择题 常温下,pH=12的氢氧化钠溶液和pH=4的醋酸溶液等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
A.混合前的醋酸约1%发生电离
B.混合后的溶液中c(Na+)=c(CH3COO-)
C.氢氧化钠和醋酸的浓度不相等
D.混合后的溶液呈中性
参考答案:A
本题解析:试题分析:A、醋酸是弱酸,存在电离平衡,pH=4的醋酸溶液中氢离子浓度是10-4mol/L。常温下,pH=12的氢氧化钠溶液和pH=4的醋酸溶液等体积混合后恰好中和,这说明醋酸浓度等于强碱氢氧化钠的浓度,即醋酸的浓度是10-4mol/L,所以混合前的醋酸约有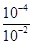 ×100%=1%发生电离,A正确;B、恰好反应时生成醋酸钠,CH3COO-水解,溶液显碱性,因此根据电荷守恒可知,溶液中离子浓度大小关系是c(Na+)>c(CH3COO-)>c(OH-)>c(H+),B不正确;C、氢氧化钠和醋酸的浓度相等,都是10-2mol/L,C不正确;D、混合后的溶液呈碱性,D不正确,答案选A。
×100%=1%发生电离,A正确;B、恰好反应时生成醋酸钠,CH3COO-水解,溶液显碱性,因此根据电荷守恒可知,溶液中离子浓度大小关系是c(Na+)>c(CH3COO-)>c(OH-)>c(H+),B不正确;C、氢氧化钠和醋酸的浓度相等,都是10-2mol/L,C不正确;D、混合后的溶液呈碱性,D不正确,答案选A。
考点:考查醋酸与氢氧化钠溶液中和后溶液酸碱性判断以及离子浓度大小比较
本题难度:困难