微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,浓度均为0.1 mol/L的6种盐溶液pH如下:
溶质
| Na2CO3
| NaHCO3
| Na2SiO3
| Na2SO3
| NaHSO3
| NaCl O
|
pH
| 11.6
| 9.7
| 12.3
| 10.0
| 4.0
| 10.3
|
下列说法正确的是
A.Cl2和Na2CO3按物质的量之比1:1反应的化学方程式为:Cl2+Na2CO3+H2O=HClO+NaHCO3+NaCl
B.相同条件下电离程度比较:HCO3->HSO3->HClO
C.6种溶液中,Na2SiO3溶液中水的电离程度最小
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3-)>c(SO32?)>c(OH-)
参考答案:A
本题解析:因为氯气与水反应是一个可逆反应,生成盐酸和次氯酸,盐酸能与碳酸氢钠反应,而次氯酸不能,盐酸反应后,使反应向正向移动,所以可增大氯水中次氯酸的浓度,A正确;B.根据表格可知:四种溶液中水电离程度最大的是碳酸钠.因为碳酸钠、碳酸钠、碳酸氢钠、次氯酸钠都是强碱弱酸盐,溶液呈碱性是由于三种盐水解的原因,所以水解程度越大,pH越大,碳酸钠的pH最大,所以水的电离程度最大,亚硫酸氢钠的溶液呈酸性,说明电离程度大于水解程度,电离出的氢离子抑制了水的电离。因此错误;C、常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3,所以错误;D.亚硫酸氢钠是强电解质完全电离,但是亚硫酸氢根离子的电离和水解都是微弱的,亚硫酸根离子的电离程度大于水解程度,所以NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),D错误。
考点:化学平衡的移动,盐类的水解与酸的电离程度的关系,盐溶液中的离子浓度大小的比较。
本题难度:一般
2、选择题 下列方程式中属于水解反应的是 ?
[? ]
A.HCO3-+H2O H3O++CO32- ?
H3O++CO32- ?
B.HCO3-+H2O OH-+H2CO3 ?
OH-+H2CO3 ?
C.NH3+H2O NH4++OH-? ?
NH4++OH-? ?
D.HCO3-+OH-==?CO32-+H2O
参考答案:B
本题解析:
本题难度:简单
3、选择题 相同状况下,等体积的下列溶液,阴离子的总浓度最大的是
A.0.2 mol/LK2S
B.0.1 mol/LBa(OH)2
C.0.2 mol/LNaCl
D.0.2 ml/L(NH4)2SO4
参考答案:A
本题解析:
本题难度:困难
4、简答题 (10分)(1)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液中,设由水电离产生的OH-的物质的量浓度分别为A和B,则A________B(填“>”、“=”或“<”)。
(2)在纯碱溶液中滴入酚酞,溶液变红色,若向该溶液中再滴入过量的BaCl2溶液,所观察到的现象是_________________________,其原因是_________________________。
(3)对于盐AmBn的溶液:①若为强酸弱碱盐,其水解的离子方程式是_______________。
②若为弱酸强碱盐,其第一步水解的离子方程式是___________________________。
参考答案:(10分)(1);<
(2)产生白色沉淀,红色逐渐褪去(两个现象各1分,意思对就给分);
钡离子与碳酸根离子结合成为难溶的碳酸钡,从而抑制了碳酸根离子的水解。(意思对就给分)
(3)An++nH2O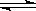 A (OH)n+nH+ Bm-+H2O
A (OH)n+nH+ Bm-+H2O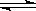 HB (m-1)- + OH-
HB (m-1)- + OH-
本题解析:(1)氢氧化钠溶液中,存在大量的氢氧根离子,对水的电离起抑制作用,而醋酸钠溶液中,醋酸根离子水解,对水的电离起促进作用,所以水电离产生的氢氧根离子的浓度A<B;
(2)纯碱为碳酸钠,因为碳酸根离子水解使溶液呈碱性,所以加入酚酞试液变红色,再滴入氯化钡溶液,因为钡离子与碳酸根离子结合为碳酸钡沉淀,使碳酸根离子的浓度减小,碳酸根离子的水解平衡逆向移动,溶液的碱性减弱,所以红色逐渐褪去,且产生白色沉淀;
(3)对于强酸弱碱盐水解时,弱碱的阳离子水解的离子方程式一步写成,所以水解的离子方程式是An++nH2O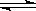 A (OH)n+nH+;对于弱酸强碱盐水解时,弱酸根离子的水解是分步写的,所以第一步水解的离子方程式是Bm-+H2O
A (OH)n+nH+;对于弱酸强碱盐水解时,弱酸根离子的水解是分步写的,所以第一步水解的离子方程式是Bm-+H2O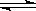 HB (m-1)-+OH-。
HB (m-1)-+OH-。
考点:考查条件对水电离的影响,水解离子方程式的书写
本题难度:困难
5、选择题 表示下列变化的化学用语正确的是
A.Na2CO3的水解:CO32-+H2O H2CO3+2OH-
H2CO3+2OH-
B.用石墨电极电解硫酸铜溶液:2Cu2++4OH- 2Cu+O2↑+2H2O
2Cu+O2↑+2H2O
C.钢铁发生吸氧腐蚀的正极反应式为:O2 +2H2O+4e- = 4OH-
D.草酸使酸性高锰酸钾溶液褪色:2MnO4―+5C2O42―+16H+=2Mn2++10CO2↑+8H2O