��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
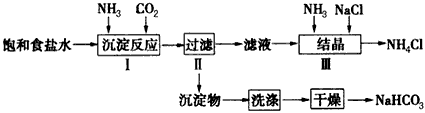
1��ʵ���� ʵ��������ȡ����NaHCO3��NH4Cl��ʵ�鲽������
��ش�
(1)Ϊ����ȡI���������õİ�����ijͬѧ�������ͼ1 ��ʾװ��
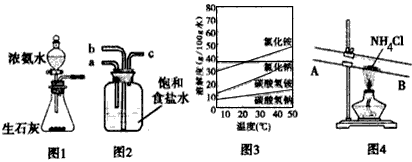
�Լ�����Ũ��ˮ������ƿ�еIJ�����_________________��
(2)����ͼ2װ�ý��иó�����Ӧ����Ӧ����ʽΪ��NaCl +NH3+CO2+H2O=NaHCO3��+NH4Cl��ʵ��ʱ�����ȴ�______���a������b����c������ͨ��__________��
(3)���������Һ��ͨ�백��������ϸСʳ�ο�������ʹNH4Cl���嵥���ᾧ������
����֪����������ʲ�ͬ�¶��µ��ܽ��������ͼ3��ʾ����ᾧʱ�˲���________��������ᾧ�� ���½ᾧ������
��ijͬѧ�������ͼ4��ʾ��װ������֤���õľ����к���NH4+��
���������ȡ����������Ӳ���Թ��У��Ծ��岿λ���ȡ�����____���A����B����������____ ��ֽ���۲�����
(4)�밴��ʾ���NaHCO3����������ʵ����ơ�
�Լ������ᡢ����ʯ��ˮ������������Һ������ˮ��������������ƽ���ձ���©�������������������ȡ�
��ȷ����ag��Ʒ����ˮ���������������������������ѡ��____��
A��Ca(OH)2��Һ B��CaCl2��Һ C��BaCl2��Һ D��Ba(OH)2��Һ
�ڹ��ˡ�ϴ�ӡ���ɣ���ȴ���������Ƶù�������Ϊbg��
���ظ����ϡ���ɣ���ȴ��������������ֱ��____ Ϊֹ����ʱ�Ƶù�������Ϊcg��
�ܼ��㣺��Ʒ��NaHCO3�ĺ���Ϊ____��
�ο��𰸣�(1)����Һ©���Ͽڻ�����ת���䰼����ڲ�С���룬�ٴ��¶�����
(2)a��NH3
(3)�ٽ��½ᾧ����A��ʪ��ĺ�ɫʯ��
(4)��D����������γ����Ľ����ͬ����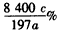
���������
�����Ѷȣ�һ��
2��ѡ���� ����Ϊ��ȡ�屽ʵ����й�����Ľ��ͺ�������������ȷ����
[? ]
A��ʵ������ȡ���屽Ϊ��ɫ��Һ�壬�������ܽ��������ɵ�
B���屽��ˮ�ᣬ����屽����ˮ����
C��ʵ������ȡ�屽ʱ�����ܿڳ��ְ��̣�������HBr��ˮ�������γɵ�
D���屽�ͱ��Ļ���������ˮ��ȡ����
�ο��𰸣�A
���������
�����Ѷȣ���
3������� ���Թ�A�м���3mL�Ҵ���Ȼ������Թܱ���������2mL�Ҵ�����ͼ���Ӻ�װ�ý���ʵ�飬����ȡ����������
��1���Թ�B��ʢ�ŵ��Լ���______����Ӧ��Ũ�����������______��
��2���Ҵ������ᷴӦ�Ļ�ѧ����ʽ��______��
��3��B�еĵ��ܲ���Դ:91������ 91exam.org�ܲ���Һ�����µ�ԭ����______��
��4����30g������46g�Ҵ���Ӧ�����ʵ�ʲ��������۲��ʵ�60%����ɵõ�������������������______g��

�ο��𰸣���1���Ʊ���������ʱ���ñ���̼������Һ����������������Ҫ���������������������ڱ���̼���ƣ��Ҵ���ˮ���ܣ������ܱ�̼�������գ����ڳ�ȥ���ʣ�Ũ������������������ȡ�е�����Ϊ����ˮ���ʹ�����
�ʴ�Ϊ������̼������Һ����ˮ����������
��2���������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ��ͬʱ�÷�Ӧ���棬��Ӧ�Ļ�ѧ����ʽΪ��CH3COOH+CH3CH2OH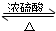 CH3COOC2H5+H2O��
CH3COOC2H5+H2O��
�ʴ�Ϊ��CH3COOH+HOCH2CH3 CH3COOCH2CH3+H2O��
CH3COOCH2CH3+H2O��
��3���ӷ�������������Ҵ������ڱ���̼������Һ�����Ȳ����������Na2CO3��Һ���������ȷ�Ӧ����Թ��У������Թ����ѣ�����B�еĵ��ܲ��ܲ���Һ�����µ�ԭ���Ƿ�ֹ������
�ʴ�Ϊ����ֹ������
��4��30g��������ʵ���Ϊ��30g��60g/mol�T0.5mol��46g�Ҵ������ʵ���Ϊ��46g��46g/mol�T1mol��
���ݷ���ʽ��CH3COOH+HOCH2CH3 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
Ӧ��������ȫ��Ӧ���������۲���������������Ϊ0.5mol������Ϊ0.5mol��88g/mol=44g��ʵ�ʲ���Ϊ0.44g��60%=26.4g��
�ʴ�Ϊ��26.4��
���������
�����Ѷȣ�һ��
4��ʵ���� ������BN����һ����Ҫ�Ĺ����մɲ��ϣ�����Ȼ��ɰΪ��ʼ�����һϵ�з�Ӧ���Եõ�BN������ͼ��ʾ��?

����H3BO3�Ʊ�B2O3�Ļ�ѧ����ʽ��_________��
��ijʵ��С������������Ӧԭ��(B2O3?+?2NH3? 2BN?+?3H2O)������װ���Ʊ�������
2BN?+?3H2O)������װ���Ʊ�������

��֪��BN�������ܱ�����������������ˮ��B2O3��������ˮ����������ˮ�� ?
��1�����Ӻ�װ�ú��ڸ����Ӵ�ͿĨ����ˮ��Ȼ��ͨ��N2��������ԡ�֤�����������õ�������_____________��ͨ��N2����һ������______________��
��2��ƿB��װ��������Һ��������_____________��
��3����Ӧ����ʱ���رյ�¯�ͻ���K���������õ��ɼмн�A��B֮�����Ƥ�ܣ�ֱ��___________��ת�Ʋ����û�мн���Ƥ�ܿ��ܹ۲쵽��������__________��
��4������ȥ������δ��Ӧ��B2O3���õ�������BN���壬ʵ�����������__________��
�ο��𰸣���2H3BO3 B2O3+ 3H2O
B2O3+ 3H2O
��1�������Ӵ�������ĭ������?��ȥװ���е�����
��2������δ��Ӧ�İ���
��3��װ����ȴ������ ��?ƿB�е�ϡ���ᵹ����ƿA�У������������𰸣�
��4�����ֲ�Ʒ������������ˮ����ֽ������ȹ��ˣ�����ˮϴ������2��3�Σ����
���������
�����Ѷȣ�һ��
5������� ��ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3������������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4��5H2O��CaCO3���������£�
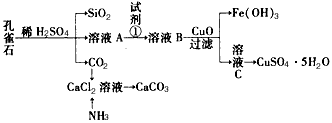
��ش��������⣺
��1����ҺA�еĽ���������Cu2+��Fe2+��Fe3+������ʵ�鲽�����Լ���Ϊ____������ĸ����ͬ����������ҺB��Fe3+������Լ�Ϊ____��
a��KMnO4
b��(NH4)2S
c��H2O2
d��KSCN
��2������ҺC���CuSO4��5H2O����Ҫ���������������ᾧ�����˵Ȳ��������ձ���©���⣬���˲�����Ҫ�õ�����һ����������________���������ڴ˲����е���Ҫ������___________��
��3��ֱ�ӽ�CO2ͨ��CaCl2��Һ���ܵõ�CaCO3������ ____________��ԭ����____________________��
�ο��𰸣���1��c��d
��2��������������
��3�����ܣ�̼������Ա�������
���������
�����Ѷȣ�һ��