微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 从某A的水溶液出发,有下图一系列变化(参加反应的水和生成的水均没有表示),已知D的焰色反应为紫色。
⑴写出化学式:A ▲ E ▲ Y ▲
⑵写出①、②反应离子方程式 ▲ , ▲
⑶Y有毒,含Y水溶液可加W检验其存在。还可向其水溶液中滴加 ▲ 检验其存在,该反应的化学方程式为: ▲ 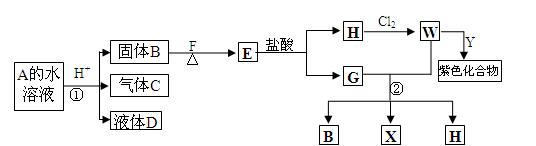
参考答案:⑴A K2S2O3 E FeS Y C6H6O
⑵① S2O32-+2H+=S↓+SO2↑+H2O
② 2Fe3++H2S=2Fe2++S↓+2H+
⑶ 过量浓溴水 ,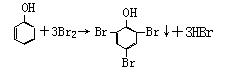
本题解析:略
本题难度:一般
2、选择题 下列化学用语或模型表示正确的是
A.H2O2分子结构式:H一O一O一H
B.氮气的电子式:N 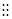 N
N
C.Mg2+结构示意图:
D.C2 H4分子比例模型: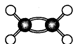
参考答案:A
本题解析:氮气的电子式为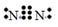 ,B项错误;Mg2+结构示意图
,B项错误;Mg2+结构示意图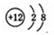 ,C项错误,D项为乙烯的球棍模型,不是比例模型。答案选A。
,C项错误,D项为乙烯的球棍模型,不是比例模型。答案选A。
点评:从近几年的考试题中可以看出,这类题主要考察的是原子(离子)的结构示意图,有机物的球滚模型或者比例模型,有机物的结构式或结构简式,原子、离子、化合物或取代基的电子式。要熟练掌握这些化学术语才能准确的回答这类问题。
本题难度:一般
3、简答题 已知:MnO2+4HCl(浓)
?MnCl2+Cl2↑+2H2O.一定质量的二氧化锰溶解在100mL过量的浓盐酸中,当反应生成?4.48L?氯气(标况)时,剩余溶液中盐酸的浓度为1mol/L(假设反应前后体积不变).请计算:
(1)反应耗用MnO2的质量
(2)被氧化的HCl物质的量
(3)原浓盐酸的物质的量浓度.
参考答案:氯气的物质的量为4.48L22.4L/mol=0.2mol,
设耗用二氧化锰xmol,参加反应的盐酸ymol,则
MnO2+4HCl(浓)??△?.?MnCl2+Cl2↑+2H2O
1?4? 1
x?y? 0.2mol
11=x0.2mol、41=y0.2mol,
解得x=0.2mol,y=0.8mol,
(1)反应耗用MnO2的质量为0.2mol×87g/mol=17.4g,
答:反应耗用MnO2的质量为17.4g;?
(2)被氧化的HCl物质的量为0.8mol×12=0.4mol,
答:被氧化的HCl物质的量为0.4mol;
(3)原溶液中HCl的物质的量为0.8mol+0.1L×1mol/L=0.9mol,
原浓盐酸的物质的量浓度为c(HCl)=0.9mol0.1L=9mol/L,
答:原浓盐酸的物质的量浓度为9mol/L.
本题解析:
本题难度:一般
4、选择题 氧化还原反应与四种基本类型反应的关系如右图所示,
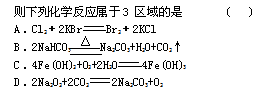
参考答案:D
本题解析:依题意可知,3区域属于氧化还原反应,排除B;而且也不能是化合反应、分解反应、置换反应,排除AC,只有D项符合题意
本题难度:简单
5、选择题 在常温常压下,取下列四种气态烃各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是( )
A.CH4
B.C2H6
C.C3H8
D.C4H10
参考答案:D
本题解析:
本题难度:简单