微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 除水电离出的H+、OH-离子外,某溶液中只含有四种离子,且浓度均为0.1mol/L,这种溶液可能是
[? ]
A.? 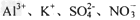
B.? 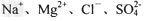
C.?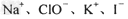 ?
?
D.? 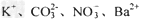
参考答案:B
本题解析:
本题难度:一般
2、计算题 (16分) 在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。则:
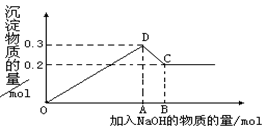
(1)写出代表各线段发生反应的离子方程式:
OD段 , _________________________________,
DC段 _。
(2)原溶液中Mg2+、Al3+物质的量浓度之比为 。
(3)图中C点表示当加入 mol NaOH时,Al3+已经转化为 Mg2+已经转化为 。
(4)图中线段OA∶AB= 。
参考答案:(共16分)
(1)Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓ ;
Al(OH)3+OH-=AlO2-+2H2O每个2分共6分
(2)2∶1(2分)
(3)0.8 (2分) 全部溶解生成NaAlO2、(2分)完全生成沉淀Mg(OH)2,(2分)
(4)7∶1 (2分)
本题解析:(1)MgCl2和AlCl3的混合溶液中,开始加入氢氧化钠,生成的是氢氧化镁和氢氧化铝沉淀,沉淀达到最高点时,镁离子、铝离子完全沉淀,此时沉淀为0.3mol,反应如下:
Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓ ;
继续加入氢氧化钠,会与氢氧化铝反应,沉淀溶解,反应如下:
Al(OH)3+OH-=AlO2-+2H2O
(2)根据从D到C,沉淀减少量为0.1mol,知道n(Al(OH)3)=n(AlCl3)=0.1mol,n(Mg(OH)2)= n(MgCl2)=0.3-n(Al(OH)3)=0.2mol;则n(Mg2+):n(Al3+)=2:1;
(3)根据方程式计算
Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓ 、Al(OH)3+OH-=AlO2-+2H2O
0.2mol 0.4mol 0.1mol 0.3mol 0.1mol 0.1mol
加入的n(NaOH)=0.4+0.3+0.1=0.8mol时,Al3+已经转化为NaAlO2,Mg2+已经转化为沉淀Mg(OH)2。
(4)根据上述的方程式计算,到D点时加入的氢氧化钠为0.7mol,从D到C加入的氢氧化钠为0.1mol,所以为7:1。
考点:考查铝离子、镁离子的转化及方程式计算。
点评:通过方程式结合图像进行化学方程式计算考查学生的分析能力及观察能力,综合性较强,难度较大。
本题难度:一般
3、选择题 下列离子在指定溶液中一定能大量共存的是? ( )
①加入Al能放出大量H2的溶液中:Na+、K+、NO、Cl-、SO
②在pH=11的溶液中:Na+、AlO、NO、S2-、SO
③由水电离的c(H+)=10-12mol・L-1的溶液中:Cl-、HCO、NO、NH、F-
④加入Mg能放出H2的溶液中:Mg2+、NH、Cl-、K+、SO
A.②④
B.①②④
C.①③④
D.①②
参考答案:A
本题解析:①在NO存在的情况下,加入Al不会生成氢气
②在碱性条件下,能大量共存
③溶液显酸性或者碱性,与HCO不能共存
④能大量共存
故选A
本题难度:一般
4、选择题 某无色溶液中,若加入溴水,溴水褪色,若加入NH4HCO3,固体溶解并产生刺激性气味的气体,则该溶液中可能大量存在的离子组是( )
A.Na+、K+、C1-、OH-
B.Na+、Mg2+、S2-、C1O-
C.H+、Na+、SO42-、NO3-
D.K+、Ca2+、OH-、SO32-
参考答案:A.溶液无色,呈碱性,加入溴水褪色,并且加入NH4HCO3,固体溶解并产生刺激性气味的气体,符合题目要求,故A正确;
B.Mg2+与S2-发生互促水解反应,且S2-与C1O-发生氧化还原反应而不能大量共存,故B错误;
C.碱性条件下H+不能大量存在,故C错误;
D.Ca2+与SO32-反应生成沉淀而不能大量存在,故D错误.
故选A.
本题解析:
本题难度:简单
5、选择题 在酸性溶液中能大量共存,并且溶液为无色透明的是( )
A.K+、Ca2+、HCO
、Cl-
B.Fe2+、Na+、NO、Cl-
C.Na+、K+、Mg2+、SO
D.Mg2+、Fe3+、Cl-、OH-
参考答案:A.因H+、HCO3-结合生成水和气体,则不能共存,故A错误;
B.因Fe2+、H+、NO3-发生氧化还原反应,则不能共存,故B错误;
C.酸性溶液中该组离子之间不反应,能大量共存,故C正确;
D.Mg2+、Fe3+分别与OH-结合生成沉淀,H+、OH-结合生成水,则不能共存,故D错误;
故选C.
本题解析:
本题难度:简单