��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��16�֣���һ��������ܱ����м���2 mol A��0��6 mo1 C��һ������B�������壮һ�������·�����Ӧ��������Ũ����ʱ��仯��ͼ(��)��ʾ������t0��t1��c(B)δ������ͼ(��)Ϊt2ʱ�̺�ı䷴Ӧ��������ѧ��Ӧ������ʱ��仯��������ĸ��θı������������ͬ��ÿ����ֻ�ı�Ũ�ȡ��¶ȡ�ѹǿ�������е�һ������������t3��t4��Ϊʹ�ô�����

��ش��������⣺
(1)��t1��15 min����t0��t1����C���ʵ�Ũ�ȱ仯��ʾ��Ӧ����Ϊ?��
(2) t4��t5�θı������Ϊ?��B����ʼ���ʵ���Ũ��Ϊ?������ƽ��ʱ��Ӧ��ƽ�ⳣ�����±���ʾ��
t1��t2
| t2��t3
| t3��t4
| t4��t5
| t5��t6
|
K1
| K2
| K3
| K4
| K5
|
��K1=?(������λС��)��
K1��K2��K3��K4��K5֮��Ĺ�ϵΪ?(�á�>������<����������)��
(3) t5��t6�α����������¶Ȳ��䣬��A�����ʵ������仯��0.01 mol�����˹����������������Ƚ�������ΪakJ��д�����¶��¸÷�Ӧ���Ȼ�ѧ����ʽ?
?��
(4)����ͬ�����£�����ʼʱ�����м���a mol A��b mol B��c mol C��Ҫ�ﵽt1ʱ��ͬ����ƽ�⣬a��b��cҪ���������Ϊ?.
�ο��𰸣�(1)0.02mol/(L��min)?(2)��ѹ?0.5mol/L? 0.84? K1=K2=K3=K4<K5
 (3) 2A(g)+B(g)?3C(g)?��H����200kJ/mol? (4) a��2c/3��2.4?��b��c/3��1.2
(3) 2A(g)+B(g)?3C(g)?��H����200kJ/mol? (4) a��2c/3��2.4?��b��c/3��1.2
�����������1����ѧ��Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ������ͼ��I��֪��15min��C��Ũ�ȱ仯����0.6mol/L��0.3mol/L��0.3mol/L����������Ϊ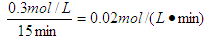
��2����ͼ����֪����t4��t5�η�Ӧ���ʼ�С����ƽ�ⲻ�ƶ������Ըı���������������¶Ⱥ�Ũ�ȣ�������t3��t4��Ϊʹ�ô��������Ըý�ֻ�ǽ���ѹǿ����˵���ı�ѹǿƽ�ⲻ�ƶ�����˷�Ӧǰ������Dz���ġ�����ͼ��I��֪A�Ƿ�Ӧ�C����������ߵı仯��֮����2�U3������Ҫʹ��Ӧǰ��������䣬Bֻ�Ƿ�Ӧ�����Ӧ�ķ���ʽΪ2A��B 3C��C��Ũ��������0.3mol/L����B��Ũ�ȼ�����0.1mol/L������B����ʼŨ����0.4mol/L��0.1mol/L��0.5mol/L����t1��t2��ƽ����ABC��Ũ�ȣ�mol/L���ֱ�Ϊ0.8��0.4��0.6������ƽ�ⳣ��Ϊ
3C��C��Ũ��������0.3mol/L����B��Ũ�ȼ�����0.1mol/L������B����ʼŨ����0.4mol/L��0.1mol/L��0.5mol/L����t1��t2��ƽ����ABC��Ũ�ȣ�mol/L���ֱ�Ϊ0.8��0.4��0.6������ƽ�ⳣ��Ϊ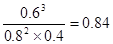 ����Ϊƽ�ⳣ��ֻ���¶��йأ�����ͼ���֪��t5��t6�Σ����淴Ӧ����ͬʱ����ƽ��������Ӧ�����ƶ�����Ϊ������ֻ�����¶����������¶ȣ����Է�Ӧ�����ȷ�Ӧ�����K1��K2��K3��K4��K5֮��Ĺ�ϵΪK1=K2=K3=K4<K5��
����Ϊƽ�ⳣ��ֻ���¶��йأ�����ͼ���֪��t5��t6�Σ����淴Ӧ����ͬʱ����ƽ��������Ӧ�����ƶ�����Ϊ������ֻ�����¶����������¶ȣ����Է�Ӧ�����ȷ�Ӧ�����K1��K2��K3��K4��K5֮��Ĺ�ϵΪK1=K2=K3=K4<K5��
��3������������жϣ�ÿ����0.01molA����Ӧ����������akJ�����Է�Ӧ���Ȼ�ѧ����ʽΪ2A(g)+B(g)?3C(g)?��H����200kJ/mol��
��4����Ϊ�����ݻ����䣨�����ݻ���2L��������Ҫʹƽ���Ч������ʼ���ʵ����ʵ�������ȵġ����������֪��ʼʱAB�����ʵ����ֱ�Ϊ2.4mol��1.2mol�����cmol��Cת��ΪAB����AB�����ʵ�����mol���ֱ���a��2c/3��b��c/3�����Թ�ϵʽ��������a��2c/3��2.4��b��c/3��1.2.
�����Ѷȣ�һ��
2��ѡ���� ��һ���Ϊ2L�ĺ����ܱ��� �������1 mol N2��4 mol H2����һ���¶��·�����Ӧ��
N2(g) +3H2(g)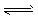 2NH3 (g)����H<0��10��ʱ�ﵽƽ�⣬ c(NH3)Ϊ0.4 mol/L������˵����ȷ����
2NH3 (g)����H<0��10��ʱ�ﵽƽ�⣬ c(NH3)Ϊ0.4 mol/L������˵����ȷ����
[? ]
A���÷�Ӧ��ƽ��ʱH2��ת����Ϊ40%
B�������¶���ʹ���������ܶ�����
C����������г���N2��ƽ�������ƶ�
D���з���Ч�����ɴ�����N2��ת����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ������ʵ��������������ԭ�����͵���
A�������Ȼ�����Һʱ����������ϡ����
B�������Ȼ�������Һʱ������������м
C���ں��з�̪�İ�ˮ�м�������NH4Cl,��Һ��ɫ���dz
D��������ͭ������Һ�м���һ�鵨�����������α����
�ο��𰸣�B
�������������ı�Ӱ��ƽ���1��������ƽ������ܹ��������ָı�ķ�����У����������������ԭ������ԭ�����������е�ƽ����ϵ��A���Ȼ�������ˮ��������ˮ�⣬���������Ȼ�����Һʱ����������ϡ�����Ŀ��������������ˮ�⣬A���������⣻B���������Ӽ��ױ��������������ӣ����������Ȼ�������Һʱ������������м��Ŀ���Ƿ�ֹ�������ӱ���������ƽ����ϵ��B�������⣻C����ˮ�д��ڵ���ƽ�⣬����ں��з�̪�İ�ˮ�м�������NH4Cl��Һ�����ư�ˮ�ĵ��룬��Һ�ļ��Խ�����ɫ���dz��C���������⣻D������ͭ����ˮ�����ܽ�ƽ�⣬���������ͭ������Һ�м���һ�鵨�����������α����D���������⣬��ѡB��
�����Ѷȣ�һ��
4������� ��6�֣�ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�

��1���÷�Ӧ�Ļ�ѧ����ʽΪ?��
��2����Ӧ��ʼ��2min������Z��ƽ����Ӧ����Ϊ?��
��3����X��Y��Z��Ϊ���壬��Ӧ��ƽ��ʱ����ʱ�����ڵ�ѹǿ����ʼѹǿ֮��Ϊ?��
�ο��𰸣���1��3X? +? Y 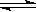 ?2Z?��2��0.05mol.(L.min)-1?��3��9:10
?2Z?��2��0.05mol.(L.min)-1?��3��9:10
�����������
�����Ѷȣ���
5��ѡ���� T���£����ݻ�Ϊ2L���ܱ������з�����ӦCO��g��+H2O��g��?CO2��g��+H2O��g�����������ݼ��±�������t2��t1����
| ��Ӧʱ��/min | N��CO��/mol | H2O/mol | N��CO2��/mol | N��H2��/mol
0
1.20
0.60
0
0
t1
0.80
t2
0.20
|
����˵����ȷ���ǣ�������
A����Ӧ��t1min�ڵ�ƽ������Ϊv��H2��=mol?L-1?min-1
B��ƽ��ʱCO��ת����Ϊ66.67%
C�����¶��·�Ӧ��ƽ�ⳣ��Ϊ1
D�������������䣬����ʼʱn��C0��=0.60?mol��n��H20��=1.20?mol����ƽ��ʱn��C02��=0.20?mol
�ο��𰸣�A���ɱ������ݿ�֪��t1min�ڲμӷ�Ӧ��CO�����ʵ���Ϊ1.2mol-0.8mol=0.4mol��v��CO��=0.4mol2Lt1min=0.2t1mol/��L?min��������֮�ȵ��ڻ�ѧ������֮�ȼ���v��H2��=v��CO��=0.2t1mol/��L?min������A����
B��t1min�ڲμӷ�Ӧ��CO�����ʵ���Ϊ1.2mol-0.8mol=0.4mol����μӷ�Ӧ��ˮΪ0.4mol����ʱˮ�����ʵ���Ϊ0.6mol-0.4mol=0.2mol��t2minʱˮ�����ʵ���Ϊ0.2mol����t1minʱ��Ӧ����ƽ�⣬��CO��ת����Ϊ0.4mol1.2mol��100%=33.3%����B����
C��t1minʱn��CO��=0.8mol��n��H2O��=0.6mol-0.4mol=0.2mol��t2minʱn��H2O��=0.2mol��˵��t1minʱ��Ӧ�Ѿ��ﵽƽ��״̬����ʱn��CO��=0.8mol��n��H2O��=0.2mol��n��CO2��=c��H2��=��n��CO��=1.2mol-0.8mol=0.4mol����Ӧǰ�������������䣬�������ʵ�������Ũ�ȼ���7ƽ�ⳣ������k=0.4��0.40.8��0.2=1����C��ȷ
D��CO��H2O�����ʵ�����1��1��Ӧ������0.60?mol?CO��1.20?mol?H2O�����1.20?mol?CO��0.6mol?H2O��ƽ��ʱ�������Ũ�ȶ�Ӧ��ͬ��t1minʱn��CO��=0.8mol��n��H2O��=0.6mol-0.4mol=0.2mol��t2minʱn��H2O��=0.2mol��˵��t1minʱ��Ӧ�Ѿ��ﵽƽ��״̬�����ݻ�ѧ����ʽ��֪�������ɵ�n��CO2��=0.4mol����D����
��ѡC��
���������
�����Ѷȣ���